Keywords
Trastuzumab; Breast cancer; HER2; Monoclonal antibodies
Introducción
El cáncer de mama es el tipo de cáncer más frecuente en la mujer [1], se presenta generalmente entre los 35 y 80 años, presentando mayor riesgo entre los 45 y 65 años.
El Receptor del Factor de Crecimiento de tipo Epidérmico Humano tipo 2 (HER2) está presente en la mayoría de las células de la glándula mamaria, y ayuda a controlar los mecanismos de crecimiento, división y reparación de las células mamarias. En uno de cada cinco casos de cáncer de mama (20%) hay una mutación en el gen que produce el receptor y debido a esta mutación, el gen de HER2 se sobre expresa, causando así la producción desmesurada de receptores. Debido a la cantidad de receptores, las células mamarias empiezan a replicarse y dividirse de manera descontrolada [2].
A estos casos se les conoce como cáncer de mama HER2-positivos (o HER2+), y en comparación con los HER2-negativos, los HER2+ tienden a ser más agresivos, crecer más rápido y su probabilidad de regresión es mayor. Además, son menos sensibles a los tratamientos convencionales de cáncer y terapias hormonales [2], por esta razón, se ha comenzado a hacer más investigación para elaborar y aprobar nuevos y eficaces tratamientos especializados para este tipo de cáncer.
El Trastuzumab [3,4] es un medicamento de anticuerpos monoclonales usado para tratar el cáncer de mama HER2+. Trastuzumab se acopla a los receptores HER2, lo que activa Linfocitos B, que reconocen al anticuerpo y atacan a las células cancerígenas. Se han hecho varios estudios que evalúan la calidad del tratamiento con este medicamento, y su combinación con otras terapias, como Lapatinib [5-7] o Docetaxel [8], pero muchos de los efectos adversos de esta terapia permanecen desconocidos, con algunas excepciones. El efecto adverso más severo del trastuzumab es la cardiotoxicidad, además se presentan otros efectos como la infiltración pulmonar [9], cefalea, artralgia, fatiga, nasofaringitis, diarrea, pirosis y nausea, vómito, tos y edema, entre otros [4]. En los casos de efectos adversos graves como la cardiotoxicidad, presentada como insuficiencia cardiaca, se debe interrumpir el tratamiento y buscar otra alternativa terapéutica.
Actualmente, el tratamiento con trastuzumab se recomienda únicamente en cáncer de mama de alto riesgo con HER2+, en estos casos las guías de tratamiento actuales [10] recomiendan la administración de antraciclina y taxanos en combinación con 6 ciclos de trastuzumab (Figura 1).
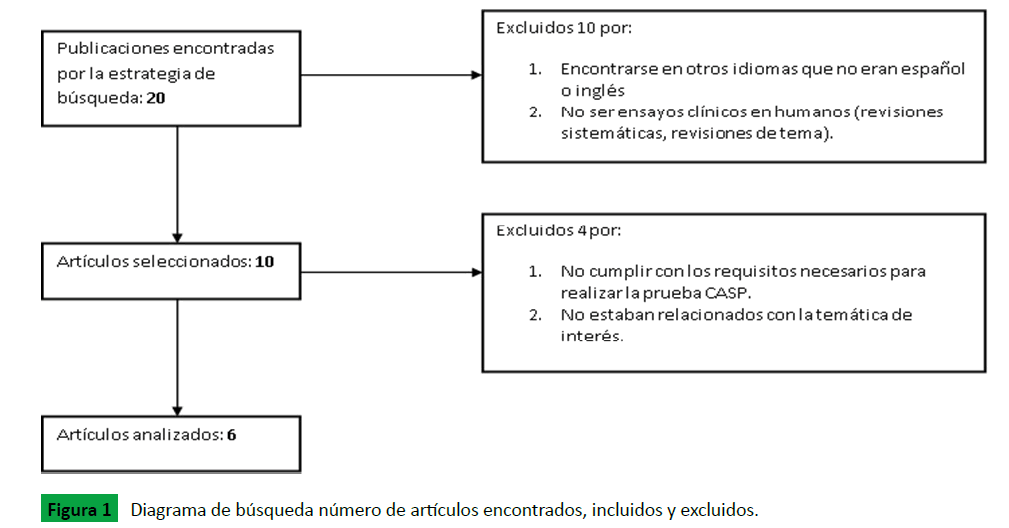
Figura 1: Diagrama de búsqueda número de artículos encontrados, incluidos y excluidos.
El objetivo de esta revisión es responder a la pregunta sobre la eficacia del tratamiento con Trastuzumab, así como su combinación con otros medicamentos sobre el cáncer de mama HER2+ y sus efectos adversos en los pacientes con este padecimiento.
Materiales y Métodos
Tipo de Estudio
Se realizó una revisión sistemática de ensayos clínicos, estudios observacionales y casos clínicos que evaluaran el tratamiento con Trastuzumab.
Criterios de Inclusión
En la revisión se incluyeron todos los artículos originales que fueran ensayos clínicos, estudios observacionales o casos clínicos que evaluaran Trastuzumab como terapia coadyuvante para el tratamiento de cáncer de mama HER2+, ya sea cirugía, quimioterapia o en combinación con otro medicamento. Se incluyeron también los artículos que evaluaran los efectos adversos de la intervención con Trastuzumab.
Se excluyeron los artículos que no cumplieran con estos criterios después de la revisión de calidad, que no fueran en humanos, o que no pasaran la prueba de calidad.
Búsqueda de publicaciones y medición de calidad
Los autores buscaron en las siguientes bases de datos: Pubmed, EBSCO, Scielo, Ovid y Cochrane, ensayos clínicos, estudios observacionales y casos clínicos en español o inglés, publicados a partir del año 2010 en revistas indexadas en el catálogo de la NLM de la NCBI (Pubmed).
Se clasificaron por tipo de publicación e idioma y se les aplico la prueba CASP (Clinical Appraisal Skills Programme) de la Universidad de Oxford [11]. Se excluyeron de la revisión aquellos artículos que no pasaran satisfactoriamente la prueba.
Extracción de datos
Los artículos incluidos en la revisión fueron repartidos de manera equitativa entre todos los autores para su lectura y extracción de resultados con datos estadísticos, efectos adversos y conclusiones pertinentes para la revisión.
Resultados
Se identificaron un total de 20 artículos, de los cuales se excluyeron 14 por tratarse de revisiones, ensayos clínicos en animales, por no pasar la prueba CASP o por no cumplir con los criterios de inclusión. Se analizaron 6 artículos que cumplieron con todos los criterios de inclusión y pasaron satisfactoriamente la prueba CASP. Estos artículos fueron 4 ensayos clínicos [6-8,12], 1 estudio observacional retrospectivo [5] y un reporte de caso [9].
Los artículos revisados utilizan al Trastuzumab combinado con otros medicamentos o tratamientos para el cáncer de mama HER2+, de estos artículos, tres usaron Lapatinib con Trastuzumab [5-7], uno usó quimioterapias, antraciclinas y Trastuzumab [12], y uno usó Pertuzumab, Docetaxel y Trastuzumab [8]. Además, se analizó un caso clínico [9] del Hospital General del Hospitalet en Barcelona, España, para el análisis de distintos efectos adversos (en este caso, infiltración pulmonar)
Las poblaciones de estudio que se incluyeron en los artículos analizados fueron personas con cáncer de mama HER2+ en todos los artículos, pero en dos se encontraban en etapas iniciales del cáncer [6,12], tres evaluaron pacientes con metástasis [5,7,8] y uno a pacientes con cáncer metastásico no resecable [9].
Los estudios que evaluaron el tratamiento combinado de Trastuzumab con Lapatinib [5-7] reportaron que la combinación de estos dos fármacos resulta en el aumento del tiempo libre de progresión del cáncer de mama HER2+ con metástasis de etapa avanzada por 3-5 meses. Uno de estos estudios [7] usó una variante de Lapatinib TM1 y se reportó el aumento del tiempo libre de supervivencia sin progresión de la enfermedad de 6-9 meses. Los efectos adversos incluyeron diarrea grado 2, vómitos, hepatotoxicidad, hipoglucemia y neutropenia.
El estudio que evaluó el uso de Trastuzumab con quimioterapia y antraciclinas [12] reportó la muerte de 348 de los 3222 pacientes en el estudio en un periodo de 65 meses, con un aumento del tiempo de supervivencia libre de progresión de la enfermedad posterior al periodo de tratamiento, además de la disminución de tamaño en tumores ≤ 2 cm. El único efecto adverso reportado fue disfunción cardiaca, que fue controlada con fármacos.
El estudio que evaluó la eficacia de la combinación de Trastuzumab con Pertuzumab y Docetaxel en pacientes con cáncer de mama HER2+ metastásico [8] reportó una mediana de 57 meses de supervivencia libres de progresión de la enfermedad a comparación del grupo placebo, con efectos cardiacos adversos que fueron controlados con otros fármacos, sin complicaciones mayores.
Calidad metodológica de los estudios analizados
De los 5 estudios clínicos analizados, todos pasaron la prueba CASP para determinar su calidad metodológica, todos reportaron el uso de consentimiento informado, aprobación por el comité de bioética de su institución y prácticas acordes con la Declaración de Helsinki [13]. Dos [8,12] reportaron ciego en el estudio, dos reportaron doble ciego [5,7]. Solo uno [6] reportó conflicto de interés presente.
Discusión
La revisión incluyó a 5322 pacientes que participaron en los estudios que se analizaron, que tenían como objetivo evaluar la eficacia del Trastuzumab combinado con otras diferentes terapias y su repercusión en el tratamiento del cáncer de mama HER2+, así como los posibles efectos adversos de estos medios de terapia.
Después de analizar los resultados de los estudios incluidos en la revisión, este artículo de revisión puede sugerir la elaboración de más ensayos clínicos para confirmar la eficacia del uso de Trastuzumab como tratamiento coadyuvante para el cáncer de mama HER2+, pero no puede recomendarlo como tratamiento alternativo debido a la escasa cantidad de artículos que cumplen con los criterios de inclusión de esta revisión y al acceso limitado a los demás artículos en las bases de datos y en las revistas.
Los resultados arrojan evidencia del potencial del Trastuzumab como tratamiento para esta enfermedad, siendo el tratamiento más óptimo la combinación de éste con Pertuzumab y Docetaxel [8] para pacientes en etapas avanzadas y con metástasis, teniendo especial cuidado con los efectos cardiacos secundarios de estos medicamentos.
Para pacientes en etapas iniciales del cáncer el tratamiento que sugiere mayor aumento del tiempo libre de progresión de la enfermedad es la combinación de Trastuzumab con quimioterapia y antraciclinas [12], teniendo pocos efectos adversos que pueden ser controlados con medicamentos.
El tratamiento con Trastuzumab y Lapatinib [5-7], aunque arroja resultados con potencial de tratamiento efectivo, tiene una gran cantidad de efectos adversos que pueden llegar a causar repercusiones permanentes o incluso la muerte del paciente [6], por lo que esta revisión no puede sugerir el tratamiento con esta combinación de fármacos.
Conclusiones
El trastuzumab es un medicamento con alto potencial terapéutico, y su uso está limitado a cáncer de mama HER2+ (con inmunohistoquímica 3+), cáncer de mama de diagnóstico temprano posterior a la cirugía o como parte del régimen de quimioterapia adyuvante.
Aunque la investigación acerca del Trastuzumab y su potencial como tratamiento coadyuvante para el cáncer de mama HER2+ existe, la gran mayoría de los artículos no cumplen con los criterios metodológicos necesarios para considerarse parte de esta revisión. Además, la escasa cantidad de artículos que cumplen con estos criterios tienen efectos únicos, por lo tanto, se requiere más investigación para demostrar el efecto real y a largo plazo que tiene este tratamiento, así como los efectos adversos a largo plazo que pueden presentar pacientes que estuvieron bajo este tratamiento.
Fortalezas y limitaciones de la revisión
Los criterios de inclusión y exclusión de esta revisión sistemática permiten mostrar los artículos que verdaderamente arrojaron resultados significativos para la comunidad científica. Pero los efectos únicos mostrados en cada artículo revisado causar dificultad para generalizar los resultados e impiden llegar a conclusiones significativas para recomendar el tratamiento con Trastuzumab para el cáncer de mama HER2+.
Implicaciones de la revisión
Para la práctica: La evidencia sugiere que el Trastuzumab como terapia coadyuvante para este tipo de cáncer tiene resultados positivos para los pacientes con esta aflicción, pero la heterogeneidad de resultados y la falta de artículos con alta calidad metodológica no permiten recomendar la terapia para estos pacientes.
Para la investigación: Se recomienda la elaboración de más estudios clínicos con alta calidad metodológica, así como metaanálisis, para la evaluación exhaustiva del Trastuzumab como tratamiento coadyuvante para el cáncer de mama HER2+.
Conflicto de Interés
No existe conflicto de interés en esta revisión sistemática por ninguno de los autores involucrados en su elaboración.
Financiamiento
Los artículos usados para esta revisión que tenían algún costo fueron comprados por el servicio de la hemeroteca de la Universidad Anáhuac México Norte.
Agradecimientos
Los autores agradecen a la Dra. Irasema Vásquez Anselmo por guiarlos en el proceso de la elaboración de esta revisión, así como a Angélica Luna Mendoza, referencia de la hemeroteca de la Universidad Anáhuac México Norte por su ayuda en la adquisición de varios de los artículos usados en esta revisión.
20055
References
- Goodman L, Hardman J, Limbird L, Gilman A (2001) Goodman & Gilman's the pharmacological basis of therapeutics. (10th edn.), New York: McGraw-Hill.
- Garnock-Jones K, Keating G, Scott L (2010) Trastuzumab. Drugs 70: 215-239.
- García-Muñoz C, Cortijo-Cascajares S, Cañamares-Orbis I, Goyache-Goñi MP, Ferrari-Piquero JM (2014) Lapatinib en combinación con trastuzumab en el tratamiento del cáncer de mama metastásico HER2 positivo: Experiencia de uso. Farm Hosp 38: 130-134.
- Baselga J, Bradbury I, Eidtmann H, Di Cosimo S, de Azambuja E, et al. (2012) Lapatinib with trastuzumab for HER2-positive early breast cancer (NeoALTTO): A randomised, open-label, multicentre, phase 3 trial. Lancet 379: 633-640.
- Verma S, Miles D, Gianni L, Krop I, Welslau M, et al. (2012) Trastuzumab Emtansine for HER2-positive advanced breast cancer. N Engl J Med 367: 1783-1791.
- Swain S, Baselga J, Kim S, Ro J, Semiglazov V, et al. (2015) Pertuzumab, Trastuzumab, and Docetaxel in HER2-Positive metastatic breast cancer. N Engl J Med 372: 724-734.
- Heras López L, Español Morales I, Losa Gaspà F, Janariz Roldán J, Bachs Carré E, et al. (2005) Infiltrado pulmonar por trastuzumab: Un cuadro de difícil diagnóstico etiológico. Rev Oncol 28: 45-49.
- Denduluri N, Somerfield M, Eisen A, Holloway J, Hurria A, et al. (2016) Selection of optimal adjuvant chemotherapy regimens for Human Epidermal Growth Factor Receptor 2 (HER2)–negative and adjuvant targeted therapy for HER2-Positive breast cancers: An American Society of Clinical Oncology Guideline adaptation of the cancer care ontario clinical practice guideline. J Clinl Oncol 34: 2416-2427.
- Slamon D, Eiermann W, Robert N, Pienkowski T, Martin M, et al. (2011) Adjuvant Trastuzumab in HER2-Positive breast cancer. N Engl J Med 365: 1273-1283.






