Palabras clave
Fenitoína. Hepatitis. Hepatitis fulminante.
Key words
Phenytoin, Hepatitis, Fulminant hepatitis.
Introducción
La fenitoína es un anticonvulsivante utilizado en una gran variedad de patologías.
Además tiene propiedades antiarrítmicas y miorrelajantes.
El mecanismo de acción terapeútica no está claro, se ha descrito su efecto sobre los canales iónicos celulares, activación del trasporte y estabilización de membrana.
La fenitoína ha sido propuesta para otros usos terapéuticos, pero su utilización ha sido limitada por sus múltiples efectos adversos e interacción con otras drogas [1].
Los fármacos y tóxicos son causas bien conocidas de fallo hepático fulminante. La hepatotoxicidad inducida por fenitoína está bien descrita pero existen muy pocos casos bien documentados de hepatitis aguda grave inducida por fenitoína [2].
Se presenta un caso de hepatitis fulminante asociada al uso de fenitoína.
Caso clínico:
Varón de 61 años sin antecedentes de interés que ingresó en el Unidad de Neurocirugía por hematoma epidural no quirúrgico tras caída secundaria a síncope. Al ingreso exploración neurológica sin focalidad (Glasgow Coma Scale 15). Inicialmente se decidió tratamiento conservador y profilaxis anticomicial con fenitoína endovenosa a dosis de 125 miligramos cada 8 horas. A las 48 horas presentó disminución del nivel de conciencia, fetor hepático y asterixis acompañados de hipotensión arterial severa, taquicardia supraventricular a 170 latidos por minuto y respiración superficial. El resto del examen físico era normal. Ante la necesidad de cuidados intensivos se decidió ingreso en la Unidad de Reanimación. Se procedió a intubación orotraqueal, inicio de ventilación mecánica y soporte vasoactivo con aminas.
Los resultados de la analítica al ingreso en reanimación fueron:
Bioquímica: glucosa 200 mg/dl, urea 28 mg/dl, creatinina 1.1 mg/dl, sodio 136 mmol/l, potasio 4.3 mmol/l, aspartato aminotrasferasa (GOT) 7163 UI/l, alanina aminotrnasferasa (GPT) 795 UI/l, gamma/glutamil transferasa (GGT) 166 UI/l, lactato deshidrogenasa 955 UI/l, bilirrubina 3 mg/dl. Hemograma: Hemoglobina 11 g/dl, hematocrito 30.2%, plaquetas 99,0 mil/ul, leucocitos 7.70 mil/ul. Coagulación: Tiempo Protrombina 19.9 seg, actividad protrombina 38%, INR 1.9.
Las serologías del virus de la hepatitis A (IgM), hepatitis B (HBsAg y anti-HBc), hepatitis C, hepatitis E, virus Herpes simplex (IgM), virus Epstein-Barr (IgM) y Citomegalovirus (IgM) fueron negativas. El RNA del virus de la hepatitis C era negativo en suero por PCR. Los anticuerpos antinucleares, antimúsculo liso y antimitocondriales fueron negativos. La cuantificación en suero de IgG, IgA, IgM, hormonas tiroideas, ferritina, ceruloplasmina y alfa-1-antitripsina estaba dentro de la normalidad.
Los niveles de fenitoína sérica fueron de 25.6 ug/ml.
La radiografía de tórax y la ecografía abdominal no mostraban anormalidades.
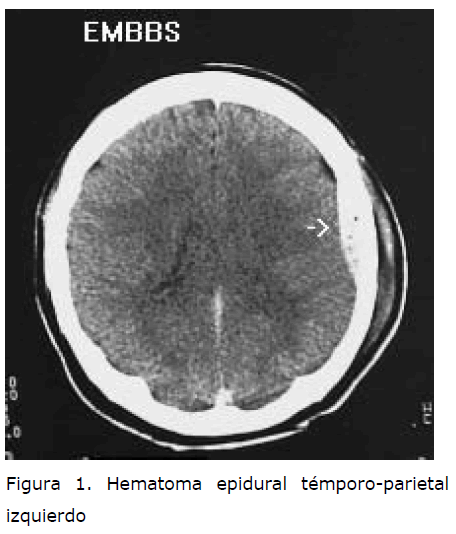
En el TAC cerebral presentaba un hematoma epidural témporo-parietal izquierdo de 10 mm de espesor ya presente el el TAC del ingreso.
Ante la sospecha de FHF inducido por fenitoína se decidió su retirada.
A partir de entonces mejoría clínica y progresiva normalización de marcadores de daño hepático, permitiendo la retirada de apoyo respiratorio y hemodinámico a los 8 días. El nivel de conciencia volvió a la normalidad.
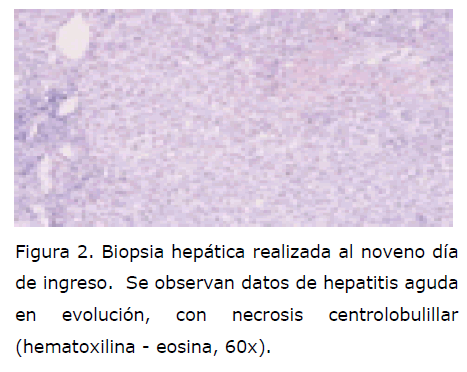
Se realiza biopsia hepática percutánea observándose datos de hepatitis aguda en evolución con necrosis centrolobulillar (Figura 2).
Figura 1. Hematoma epidural témporo-parietal izquierdo
Figura 2. Biopsia hepática realizada al noveno día de ingreso. Se observan datos de hepatitis aguda en evolución, con necrosis centrolobulillar (hematoxilina - eosina, 60x).
Dada la resolución del cuadro se decidió su traslado a la Unidad de Neurocirugía. El posterior seguimiento confirmó la total resolución de las anomalías bioquímicas.
Discusión
La fenitoína fue sintetizada en 1908 por Bilz, pero su actividad anticonvulsivante no fue descubierta hasta 1938. Desde entonces es el fármaco más utilizado para el tratamiento de las convulsiones, estando indicada en las crisis tonicoclónicas generalizadas, crisis parciales, convulsiones focales y neuralgia del trigémino. Aunque químicamente esta relacionada con los barbitúricos, no pertenece a esa clase de fármacos. La fenitoína tiene también propiedades antiarritmicas tipo IB y fue el antiarrítmico de elección en la intoxicación digitálica antes de la utilización de los fragmentos Fab [1]. La fenitoína es un ácido débil con un pKa de 8.3. Su absorción en un medio ácido como el estómago es muy baja, absorbiéndose fundamentalmente en el duodeno. Los niveles pico se alcanzan de dos a ocho horas después de la administración de una dosis oral. En los casos de intoxicación, la absorción puede mantenerse hasta 7 días después, debido a la disminución del vaciamiento gástrico y a la formación de farmacobezoar [3].
El 90% de la fenitoína se metaboliza a nivel del sistema enzimático microsomial hepático. El principal metabolito, es un derivado parahidroxifenilo que es inactivo. Seguidamente, los metabolitos sufre un proceso de glucuronoconjugación siendo excretados por la bilis y posteriormente por la orina.
Los efectos adversos producidos por la fenitoína son relativamente frecuentes y presentan gran variedad de manifestaciones. Pueden afectar al tracto gastrointestinal: vómitos, constipación, dolor epigástrico, anorexia y pérdida de peso; al sistema nervioso central: nistagmo, confusión mental, ataxia, visión borrosa, diplopía, insomnio y dolor de cabeza, o afectaciones cutáneas: rash morbiliforme y raramente dermatitis de distintas etiologías, lupus eritematoso o incluso síndrome de Stevens Johnson. Es conocida también la hiperplasia gingival producida por fenitoína, la hipertricosis o afectaciones hepáticas de distinta gravedad [4,5].
Existe una alta variabilidad genética en la tasa de metabolización de este fármaco. Generalmente, los niños lo metabolizan rápidamente, y por lo tanto su vida media es más corta que en los adultos. En estos últimos, la vida media de la fenitoína es de 22 horas. Aunque esto es extraordinariamente variable, con un rango entre 4 horas y varios días. Esto puede ser debido a disfunción hepática, inducción enzimática o factores genéticos.
Estas manifestaciones, por lo general, remiten al suspender el tratamiento, aunque en la literatura se encuentran descritos varios casos con un desenlace fatal [2,6].
La hepatitis inducida por fenitoína fue descrita por primera vez en 1941 por Mandelbam et al., tres años después de su introducción como fármaco anticonvulsuvante. Su incidencia es menor del 1% [7]. De acuerdo con una reciente revisión de 50 casos de hepatotoxicidad por fenitoína, su aparición en adultos se produce dentro de las seis primeras semanas de terapia. La distribución por edades es similar, y su incidencia es mayor en gente de raza negra. El daño hepático es principalmente citotóxico, con una necrosis extensa hepatocelular, aunque la hepatitis colestásica y granulomatosa también han sido descritas. Establecer el diagnóstico puede ser difícil, y requiere la exclusión de otras causas de daño hepático. La biopsia hepática es la principal prueba usada en el diagnóstico. En nuestro paciente la biopsia hepática mostraba cambios compatibles con el diagnóstico de hepatitis inducida por drogas, con necrosis hepatocelular, inflamación e infiltración portal por linfocitos y eosinófilos y algunas lesiones granulomatosas. El mecanismo de la hepatotoxicidad es desconocido aunque se han propuesto diferentes teorías, entre las más comunes destacan la hipersensibilidad y la formación de metabolitos tóxicos [8,9,10].
Se presenta un caso de hepatitis aguda grave inducida por fenitoína demostrada histológicamente en el que se descartan otras posibles causas: infecciosas, tóxicas, inmunológicas y metabólicas. Los datos de encefalopatía aguda como signo de insuficiencia hepática, el descenso en la tasa de protrombina permitirían clasificarlo como fallo hepático fulminante de acuerdo con los criterios de O´Grady [11].`
Bibliografía
- Donna Seger. Phenytoin and other anticonvulsants. En: Hadda Lester M, Winchester James F. Philadelphia. W.B. Saunders: 1990; 877-893.
- Lee T J, Carney C N, Lapis J L, Higgins T y Fallon H J. Dyfhenylhydantoyn-induced hepatic necrosis. Gastroenterol 1976; 70: 422- 424.
- Earnest MP, Marx JA, Drury LR. Complications of intravenous phenytoin for acute treatment of seizures:Recomendations for usage. JAMA 1983; 249: 762-765.
- Silverman A K, Fairley J, Wong R C, Dallas T X, Rochester N Y y Davis C A. Cutaneous and inmunologic reactions to phenytoin. J Am AcadDermatol 1988; 18: 721-41.
- Haruda F. Phenytoin hypersensitivity: 38 cases. Neurology 1979; 29: 1480-1485.
- Pezzimeenti J F y Hahn A L. Anicteric hepatitis-induced by diphenylhydantoin. Arch Inter Med 1970;125: 118-20.
- Mandelbaum H, kane L J. Dilantin sodium poisoning: report of case with dermatitis exfoliativa, pyrexia and hepatic an splenic enlargement. Archive Neurology Psychiatric. 1941; 45: 768- 771.
- Smythe M A, Umstead G S. Phenytoin hepatotoxicity: a review ofthe literature. Drug intell and clin Pharm. 1989; 23: 13-18.
- Prosser T R, Lander R D. Phenytoininduced hypersensitivity reactions. Clinical Pharmacy. 1897; 6: 728-734.
- Korman L B, Olson M J. Phenytoininduced hepatitis, rhaddomyolisis and renal dysfunction. Dlinical Pharmacy 1989; 8: 514-515.
- O’Grady J, Schalm R, Williams R. Acute liver failure: redefining the syndromes. Lancet 1993; 33: 273-5.
1181