Keywords
Atrial fibrillation, antiarrhythmics, clinical practice guidelines, oral anticoagulation.
Introducción
Definición y epidemiología
La fibrilación auricular (FA) es la arritmia cardíaca más frecuente en la práctica clínica [1] con un fuerte incremento en la morbimortalidad representada por la elevada tasa de ictus cardioembólicos e insuficiencia cardiaca (IC) que produce. Los últimos estudios han contribuido a mejorar el pronóstico de la enfermedad gracias a mejores estrategias de diagnóstico y tratamiento (anticoagulación y control del ritmo o de la frecuencia cardíaca con fármacos antiarrítmicos) y adaptadas a las necesidades individuales de cada paciente.
El objetivo de publicación de esta guía es presentar todas las evidencias relevantes sobre el diagnóstico y tratamiento de la FA en base a las recomendaciones y niveles de evidencia actuales [2] (Tablas 1 y 2).
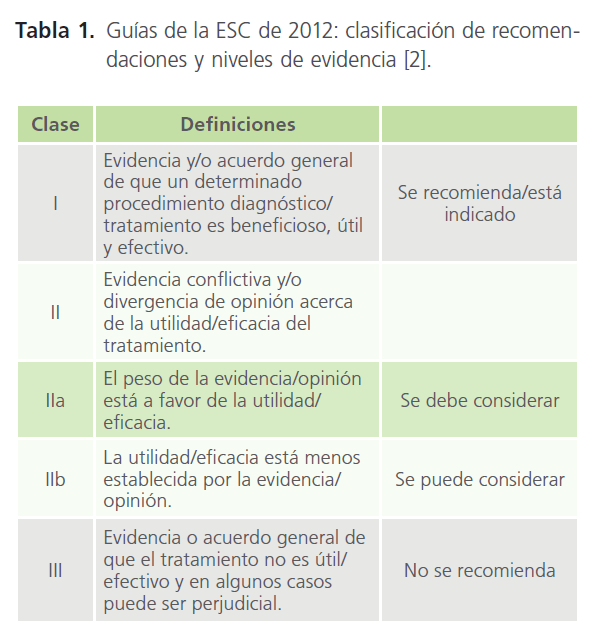
Tabla 1: Guías de la ESC de 2012: clasificación de recomendaciones y niveles de evidencia [2].

Tabla 2: Guías de la ESC de 2012: clasificación de niveles de evidencia [2].
La FA consiste en una desorganización completa de la activación eléctrica auricular, producida por automatismo y desencadenada por factores arritmogénicos (trigger) lo cual genera elevada frecuencia auricular y, si hay pérdida de la función de marcapasos en el nodo sinusal, frecuencias ventriculares de 160 a 200 latidos por minuto (lpm) o incluso mayores. La prevalencia en la población general es de un 1-2%, sin embargo, el hecho de que pueda cursar de manera asintomática y que la mayoría de los estudios epidemiológicos se hayan hecho en pacientes con FA permanente o no transitoria hace que su prevalencia real sea mayor [3, 4], incrementándose con la edad desde el 0,1% en los menores de 50 años hasta el 4-5% en los mayores de 65 años y el 9% en los mayores de 80 años [1], aunque existen estudios con una prevalencia superior al 20% en los mayores de 80 años [5]. Independientemente del rango de edad, la FA es ligeramente más frecuente en varones que mujeres [6].
En la mayoría de las ocasiones cursa de manera asintomática, aunque está asociada a una tasa aumentada de mortalidad. Suele detectarse accidentalmente por sus complicaciones más frecuentes: ictus o IC [7]. Se puede presentar asociada a diabetes mellitus (DM), hipertensión arterial (HTA) o cardiopatía estructural. Se estima que 1 de cada 5 ictus isquémicos están asociados a la presencia de FA independientemente de la edad del paciente y este riesgo se multiplica por 18 sí, además de la FA hay cardiopatía estructural. La proporción de accidente cerebrovascular (ACV) atribuible a la existencia de FA es del 7% a los 60 años y del 30% a los 90 años, ocasionando un deterioro relevante en la calidad de vida de los pacientes. La FA constituye un grave problema de salud pública debido a la prevalencia creciente, al impacto en la supervivencia y la calidad de vida y a los elevados costes sanitarios que conlleva.
Diagnóstico, clasificación y manejo inicial de la fibrilación auricular
Diagnóstico
El diagnóstico de la FA suele cursar de forma accidental, pero ante la presencia de disnea de reposo, dolor torácico, palpitaciones, síncope, mareo o ictus (accidente isquémico transitorio (AIT) y ACV) habrá que descartar la existencia de FA subyacente [7]. Se recomienda screening para FA en pacientes ≥ 65 años mediante la exploración del pulso periférico seguido de un electrocardiograma (ECG) en aquellos con pulso irregular [2] (I,B).
El diagnóstico se efectúa con la realización de un ECG de 12 derivaciones (I,B) o de 30 segundos en tira de ritmo [3]. En él, se observa que carece de onda P, aparecen ondas rápidas de fibrilación de distinta forma, tamaño y ritmo (ondas ‘f’), que conllevan una respuesta ventricular irregular. Además, para realizar un correcto análisis de las causas y complicaciones es preciso realizar estudios analíticos (hemograma, determinación de la función renal y hepática, glucemia en ayunas, perfil tiroideo y análisis de orina con determinación de microalbuminuria), radiología de tórax, monitorización con Holter (IIa,C) (indicada en FA paroxística, para evaluar el grado de control de la FA durante la actividad habitual), prueba de esfuerzo (IIa,C) (para detectar isquemia cuando esté indicado, para evaluar el control de la FA con el ejercicio en la FA permanente y para diagnosticar FA mediada por el ejercicio) y ecocardiograma (transtorácico indicado para cardiopatía estructural y transesofágico para descartar la presencia de trombos previo a la cardioversión).
Existe la necesidad de realizar una aproximación inicial para determinar si la FA es sintomática, fecha de aparición, frecuencia, duración, severidad y características de los episodios así como enfermedades asociadas y factores precipitantes.
Clasificación
Basándose en la presentación y duración de la arritmia la FA se clasifica en cinco tipos:
• Primer episodio de FA: aquella que se presenta por primera vez, independientemente de la duración de la arritmia o de la presencia y gravedad de los síntomas relacionados con la FA.
• FA paroxística: es autolimitada, normalmente, menos de 48h, aunque los paroxismos pueden durar hasta siete días. Después de 48h la probabilidad de conversión espontánea es baja.
• FA persistente: cuando el episodio de FA dura más de 7 días o cuando se precisa terminarlo por cardioversión (farmacológica o eléctrica).
• FA persistente de larga duración: es aquella que ha durado 1 año o más en el momento en que se decide adoptar una estrategia de control del ritmo.
• FA permanente: ritmo estable en FA, aceptada por el paciente y el médico donde las intervenciones de control del ritmo no son un objetivo. Si se decide control, se redefine la arritmia como FA persistente de larga duración.
La FA silente o asintomática puede tener lugar por una complicación relacionada con la FA o puede ser diagnosticada por un ECG oportuno; se puede presentar en cualquiera de las formas temporales de la FA.
Según su etiología la FA se puede clasificar en:
• Aislada o solitaria: se aplica a individuos <60 años sin evidencia clínica, ECG o ecocardiográfica de enfermedad estructural. Pueden incluirse en los grupos de FA paroxística o permanente, con FA sintomática relacionada con diversos factores (sueño, ejercicio, alcohol, comidas, historia familiar). Son pacientes que inicialmente tienen un pronóstico favorable en cuanto al riesgo de tromboembolias y de mortalidad [8].
• Asociada a cardiopatía:
Valvular: valvulopatía mitral reumática, prótesis valvular o reparación valvular.
No valvular: miocardio, pericardio, enfermedad del seno, cardiopatía isquémica, Wolff Parkinson White (WPW), defecto tabique interauricular, mixoma auricular, entre otros.
Causas no cardíacas: HTA, tirotoxicosis, infecciones agudas, depleción electrolítica, cáncer de pulmón, otros problemas intratorácicos, embolismo pulmonar, DM, síndrome de apnea del sueño.
Relacionados con la dieta y estilos de vida: sobrecarga emocional o física, consumo excesivo de cafeína, consumo excesivo de alcohol, consumo de cocaína, obesidad.
Post-cirugía cardiotorácica.
Manejo inicial
El manejo inicial se asienta en realizar una historia clínica rigurosa ante sospecha de FA o FA conocida. Los objetivos prioritarios son:
• Clasificar el grado de sintomatología (I,B): la interferencia con la actividad diaria será prioritaria para el abordaje terapéutico. Se ha propuesto la clasificación EHRA [9] (European Hearth Rhythm Association) que proporciona una puntuación creciente en función del grado de sintomatología (Tabla 3).

Tabla 3: Escala EHRA (European Hearth Rhythm Association).
• Estimación del riesgo de ACV y búsqueda de factores predisponentes (edad, HTA, DM o enfermedad arteriosclerótica). La estimación del riesgo se basa en la utilización inicialmente de la escala CHADS2 [3] (Tabla 4).

Tabla 4: Escala CHADS2
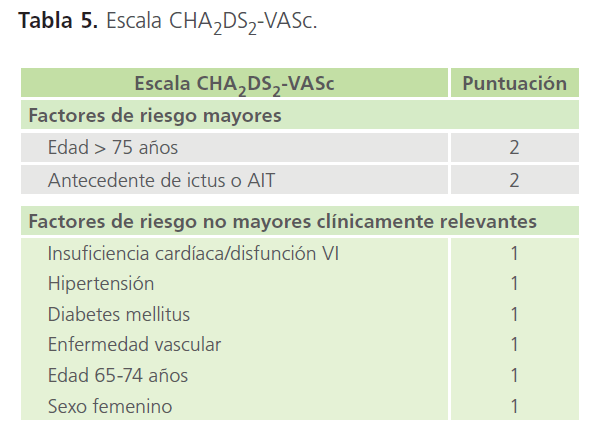
Tabla 5: Escala CHA2DS2-VASc.
Es necesario evaluar el riesgo de hemorragia cuando se prescribe tratamiento anticoagulante (I,A). Antes de iniciar tratamiento anticoagulante y en el caso de pacientes ancianos pluripatológicos es preciso cuantificar el riesgo de complicaciones hemorrágicas mediante la escala HASBLEED [10] (IIa,B) (Tabla 6).
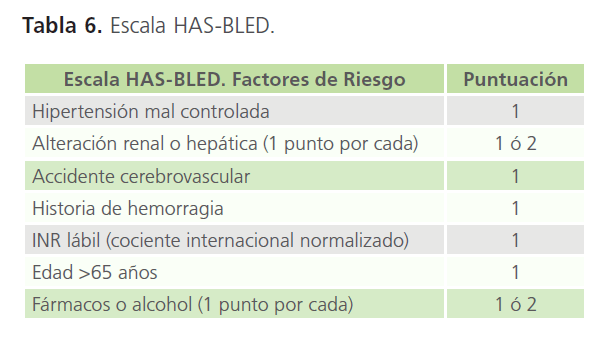
Tabla 6: Escala HAS-BLED.
• Identificar los posibles desencadenantes y complicaciones (aumento de la mortalidad, hospitalizaciones, disfunción cognitiva, función ventricular izquierda, calidad de vida y capacidad para el ejercicio).
Es preciso adaptar la estrategia terapéutica del paciente al paso de los años reevaluando el grado de sintomatología (escala EHRA) y vigilando los factores desencadenantes de complicaciones hemorrágicas. Se revisará la frecuencia cardíaca, la situación funcional, control analítico con pruebas de función hepática, renal y tiroidea (en relación especialmente con amiodarona) así como control mensual del INR en anticoagulados con antagonistas de la vitamina K (AVKs) [8]. Se evaluará la aparición de comorbilidades que no existían como DM o HTA, que obligaría a reevaluar el riesgo de taquimiocardiopatía, embolismo, IC y la necesidad de anticoagulación o marcapasos (por pausas o disfunción sinusal). Es necesaria la realización de un ECG en cada visita para vigilar alteraciones de la conducción.
Tratamiento de la fibrilación auricular
El abordaje fundamental del tratamiento de la FA se basa en reducir los síntomas y prevenir las complicaciones graves. La prevención de las complicaciones relacionadas con la FA reside en el tratamiento antitrombótico, el control de la respuesta ventricular y el tratamiento correcto de las enfermedades cardíacas concomitantes. Es necesario un adecuado manejo tanto en la fase inicial como a mediano y largo plazo, adaptando las estrategias a los cambios que pueda sufrir el paciente con el paso de los años.
Tratamiento anticoagulante
La prevención de los ACV cardioembólicos es un aspecto fundamental en el manejo de los pacientes con FA. Los fármacos anticoagulantes deben formar parte del tratamiento excepto en aquellos pacientes con bajo riesgo (FA aislada y edad <65 años) o con contraindicaciones (I,A). La elección del fármaco estará basada en el riesgo absoluto de ACV, en el riesgo de hemorragia y en la relación riesgo-beneficio [1], de tal manera que todos los pacientes en los que el riesgo de embolia sea superior al riesgo de sangrado deben recibir tratamiento anticoagulante a largo plazo [8]. Sin embargo, este tratamiento no está exento de complicaciones, algunas de ellas graves e incapacitantes, como es el caso de la hemorragia intracraneal.
Todos los pacientes con una puntuación ≥2 según la escala CHA2DS2-VASc son candidatos a tratamiento anticoagulante: nuevos anticoagulantes orales (NACOs) o AVKs. Los pacientes con una puntuación de 1 tendrán indicación de AVKs o AAS, aunque priorizando la opción de anticoagulación y los pacientes con puntuación de 0, AAS o nada (preferiblemente la segunda opción) (Tabla 7).
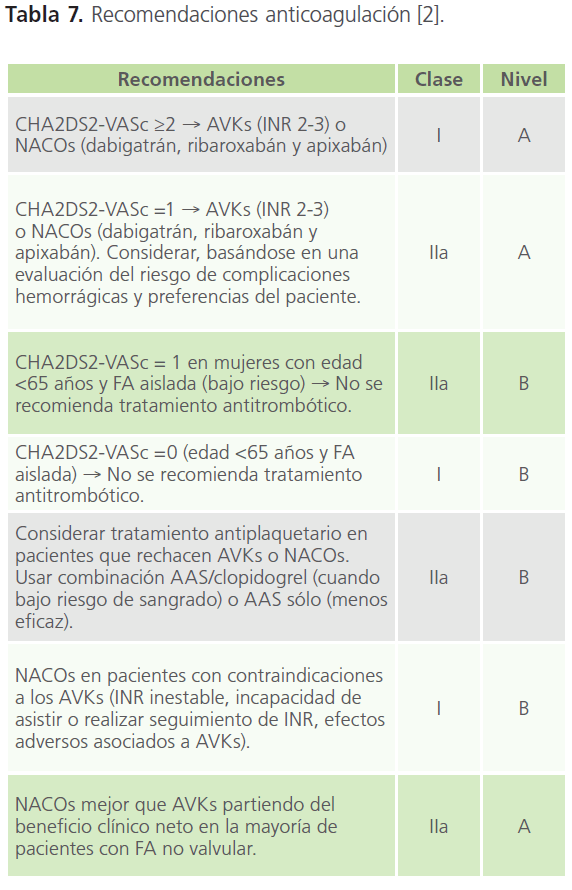
Tabla 7: Recomendaciones anticoagulación [2].
En pacientes con alguna contraindicación o riesgo especial asociado al uso de los AVKs, la alternativa ha sido el tratamiento con antiagregantes plaquetarios, pero el tratamiento anticoagulante es más efectivo que la antiagregación en la reducción del riesgo de ictus y otros accidentes vasculares mayores en los pacientes con FA no valvular. La anticoagulación comparada con placebo reduce de manera significativa la incidencia de ictus y es tres veces más efectiva que el AAS. El AAS, siendo menos efectivo que los AVKs en pacientes con FA no valvular, es mejor que placebo, sin embargo, no hay suficientes datos para apoyar el uso de AAS en la mayoría de estos pacientes ya que el riesgo de sangrado puede ser mayor que el escaso beneficio que proporciona. En los casos en que esté contraindicada la anticoagulación o la indicación no sea firme (CHA2DS2-VASc=1) se puede optar por el tratamiento antiagregante aunque a costa de menor efectividad. En caso de intolerancia o alergia a AAS se podría administrar clopidogrel.
El riesgo de complicaciones hemorrágicas se cuantifica mediante la escala HAS-BLED (II,B). Así, una puntuación HASBLED ≥3 indica riesgo elevado de hemorragia, aunque no implica necesariamente una contraindicación de anticoagulación, pero sí un seguimiento más exhaustivo (IIa,A). Se valoraría la administración de NACOs a la vista de su eficacia en la presencia de ictus y embolia sistémica, aunque menor tasa de hemorragia intracraneal y episodios hemorrágicos mayores en relación con los AVKs. HAS-BLED no debe utilizarse para excluir a pacientes del tratamiento anticoagulante (IIa,B). Los pacientes con puntuaciones HAS-BLED más altas pueden presentar una mayor reducción absoluta del riesgo de ictus que los que presentan menor riesgo de hemorragia. El riesgo de hemorragia grave con tratamiento antiplaquetario (terapia de combinación AAS/clopidogrel y sobre todo, en ancianos, también con la monoterapia con AAS) debe ser considerado similar al tratamiento anticoagulante (IIa,B).
Antagonistas de la vitamina k y nuevos anticoagulantes orales
El tratamiento anticoagulante en la FA plantea distintas opciones terapéuticas. Durante los últimos 60 años los AVKs (acenocumarol y warfarina) han sido la única alternativa. Los estudios demuestran que la anticoagulación con AVKs a dosis ajustadas en función del INR 2-3 en pacientes con FA reducen de manera significativa el riesgo de ictus cuando se comparan con AAS o con placebo [12].
Sin embargo, el uso de AVKs presenta inconvenientes: precisan de monitorización del tiempo de protrombina (TP), habitualmente expresado como cociente internacional normalizado (INR), riesgo potencial elevado (a veces sobrepercibido) de interacciones con otros fármacos y alimentos (metabolización vía citocromo P-450) y hemorragias graves, que han llevado tradicionalmente a la infrautilización de los AVKs en pacientes con FA, si bien la fracción de pacientes tratados ha ido creciendo considerablemente con el tiempo. El problema más grave de seguridad de los AVKs es el riesgo de sangrado mayor, tipo de hemorragia que hace necesario la hospitalización, la transfusión o la cirugía y la hemorragia en localizaciones anatómicas sensibles como el cerebro, con un riesgo de mortalidad o de secuelas incapacitantes mayor que en otras zonas [11]. El ajuste de dosis de anticoagulación para minimizar el riesgo de sangrado es particularmente relevante en los pacientes mayores con FA. La máxima protección contra ACV isquémicos en pacientes con FA se alcanza posiblemente con el INR entre 2 y 3.
Debido a la complejidad que supone el empleo de AVKs en la práctica clínica habitual, en la última década se ha desarrollado una amplia actividad investigadora que ha conducido a la introducción de nuevos anticoagulantes orales (NACOs): los inhibidores directos de la trombina (dabigatrán) y del factor Xa (rivaroxabán y apixabán) que no poseen los inconvenientes de los AVKs (aunque carecen de antídoto, son más costosos, y alguno de ellos con posología dos veces al día). Se caracterizan por presentar un rápido inicio de acción, bajo potencial de interacciones farmacológicas y alimentarias y un efecto anticoagulante predecible que evita la necesidad de monitorizar la coagulación [13, 14, 15, 16] (Tabla 8 y 9).
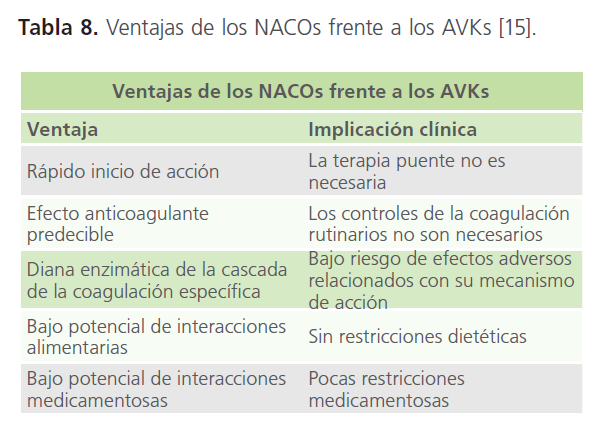
Tabla 8: Ventajas de los NACOs frente a los AVKs [15].
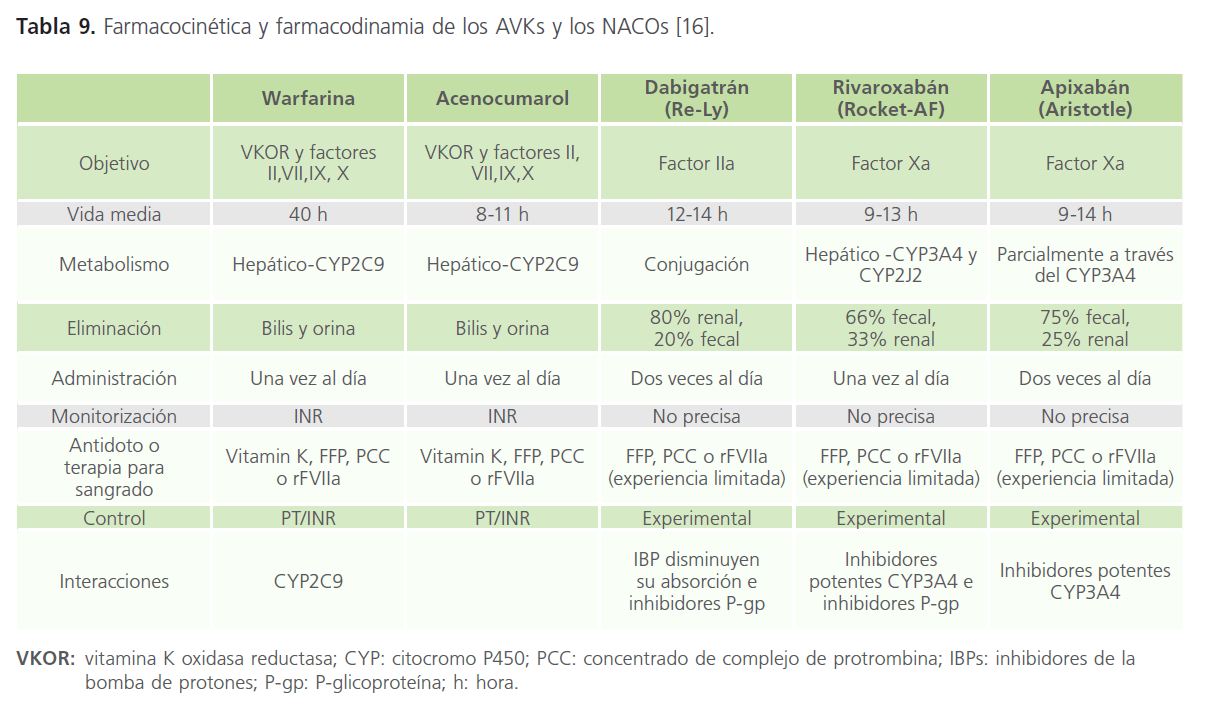
Tabla 9: Farmacocinética y farmacodinamia de los AVKs y los NACOs [16].
Recomendaciones de anticoagulación oral en pacientes con FA no valvular
Las principales recomendaciones de uso son [2]:
A) Pacientes tratados con AVKs
Mantener tratamiento con AVKs en pacientes con buen control del INR (tiempo en rango terapéutico ≥66% [17]), antecedentes de hemorragia gastrointestinal o presencia de patologías digestivas que incrementen el riesgo de sangrado.
Cambio a NACOs en pacientes con mal control del INR (el mal control no tiene que estar motivado por una mala adherencia), pacientes con ictus isquémico con criterios de alto riesgo de hemorragia intracraneal (HAS-BLED ≥3) y al menos uno de los siguientes factores: leucoaraiosis grado III-IV y/o microsangrados corticales múltiples y alergia o hipersensibilidad demostrada a cumarínicos, reacciones adversas graves a AVKs, contraindicaciones a AVKs o interacciones farmacológicas relevantes, de difícil control a pesar del ajuste posológico en función del INR e incluso la propia elección del paciente, sufragando él mismo su coste.
Los NACOs son una alternativa a los AVKs en pacientes con episodios tromboembólicos o hemorrágicos graves a pesar de un buen control del INR.
B) Pacientes con indicación de tratamiento anticoagulante que inician terapia antitrombótica
Iniciar tratamiento con AVKs excepto en casos de alergia o hipersensibilidad a cumarínicos, contraindicación específica a AVKs, antecedentes de hemorragia intracraneal, ictus isquémico con criterios de alto riesgo de hemorragia intracraneal (HAS-BLED ≥3) y al menos uno de los siguientes factores: leucoaraiosis grado III-IV y/o microsangrados corticales múltiples. Sin embargo, no hay suficiente evidencia para decir si es mejor retirar ACO cuando el riesgo es alto o es mejor mantenerlo con INR más frecuentes o en rango bajo de la normalidad.
C) Pacientes candidatos a tratamiento anticoagulante con NACOs
Tanto dabigatrán como rivaroxabán y apixabán se consideran alternativas terapéuticas válidas. La prescripción de NACOs debe ajustarse estrictamente a las indicaciones y posología recogidas en ficha técnica (son necesarios ajustes de dosis en pacientes con aclaramiento de creatinina 30-49 ml/min y HAS-BLEED ≥3). El cumplimiento y la adherencia al tratamiento es crucial dada su corta vida media.
D) Pacientes tratados con NACOs
Valorar cambio a AVKs en casos de sospecha de bajo grado de adherencia al tratamiento, hemorragia digestiva durante el tratamiento con los NACOs, contraindicación o interacción farmacológica relevante que desaconseje el uso de los NACOs.
Control de la respuesta ventricular (ritmo y frecuencia cardíaca)
Los pacientes con FA con una frecuencia inadecuada y una irregularidad del ritmo pueden presentar síntomas y trastornos hemodinámicos graves. La elección de una u otra estrategia se asienta en los factores de riesgo y en la mortalidad asociada; y se realizará de manera individualizada [18]. Varios estudios, AFFIRM y RACE no encontraron diferencias entre las estrategias de tratamiento de control de la frecuencia o de control del ritmo en relación con la mortalidad, la calidad de vida y el coste-efectividad. Existe algún estudio posterior que parece indicar que el control del ritmo es más beneficioso en pacientes con FA sintomática [19].
Control del ritmo
El control del ritmo puede ser necesario en pacientes con FA paroxística o persistente con el objetivo de eliminar los síntomas, mejorar la capacidad de ejercicio o prevenir la miocardiopatía inducida por taquicardia (taquimiocardiopatía) secundaria a la FA. Estaría indicado en pacientes <55 años o con tiempo de evolución inferior a 3 meses. Pacientes >70 años, tiempo de evolución de la FA >3 meses, crecimiento de la aurícula izquierda y/o cardiopatía reumática son considerados factores de riesgo de recurrencia lo que conlleva menor éxito en la cardioversión, no obstante, en la actualidad se recomienda intentar restablecer el ritmo sinusal en todos los pacientes que no tienen contraindicación para ello [16].
Los casos de control de ritmo son:
A) Cardioversión farmacológica
Indicada en episodios con evolución inferior a 48 h, pudiéndose realizar con flecainida, propafenona, amiodarona y vernakalant (I,A) (Tabla 10). En pacientes con FA ≤7días y cardiopatía estructural moderada puede considerarse la administración de vernakalant intravenoso (IIb,B). Si existe cardiopatía estructural significativa, es de elección amiodarona, preferentemete vía IV, ya que aumenta la probabilidad de revertir a ritmo sinusal a pacientes hemodinamicamente estables [20]. La tasa de conversión con fármacos antiarrítmicos es menor que la obtenida con cardioversión eléctrica, pero no precisa de sedación y puede facilitar la elección del tratamiento farmacológico antiarrítmico para prevenir la FA recurrente (Figura 1).
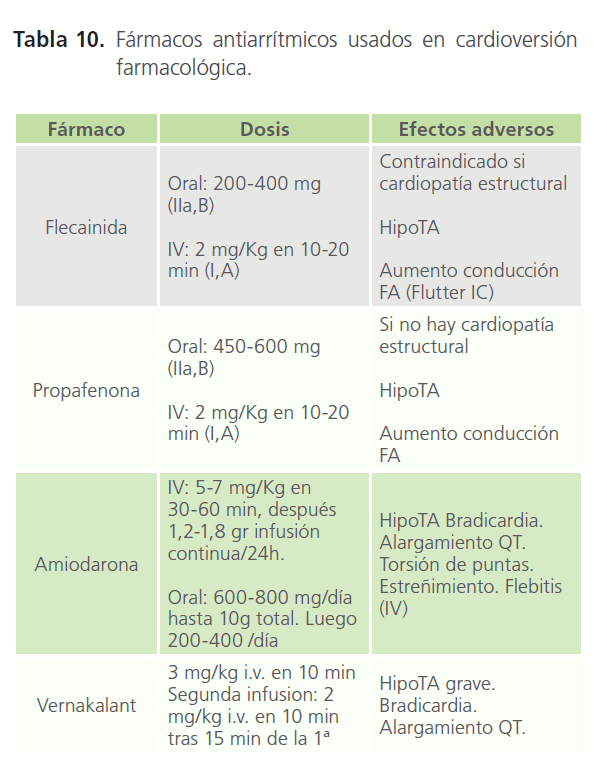
Tabla 10: Fármacos antiarrítmicos usados en cardioversión farmacológica.
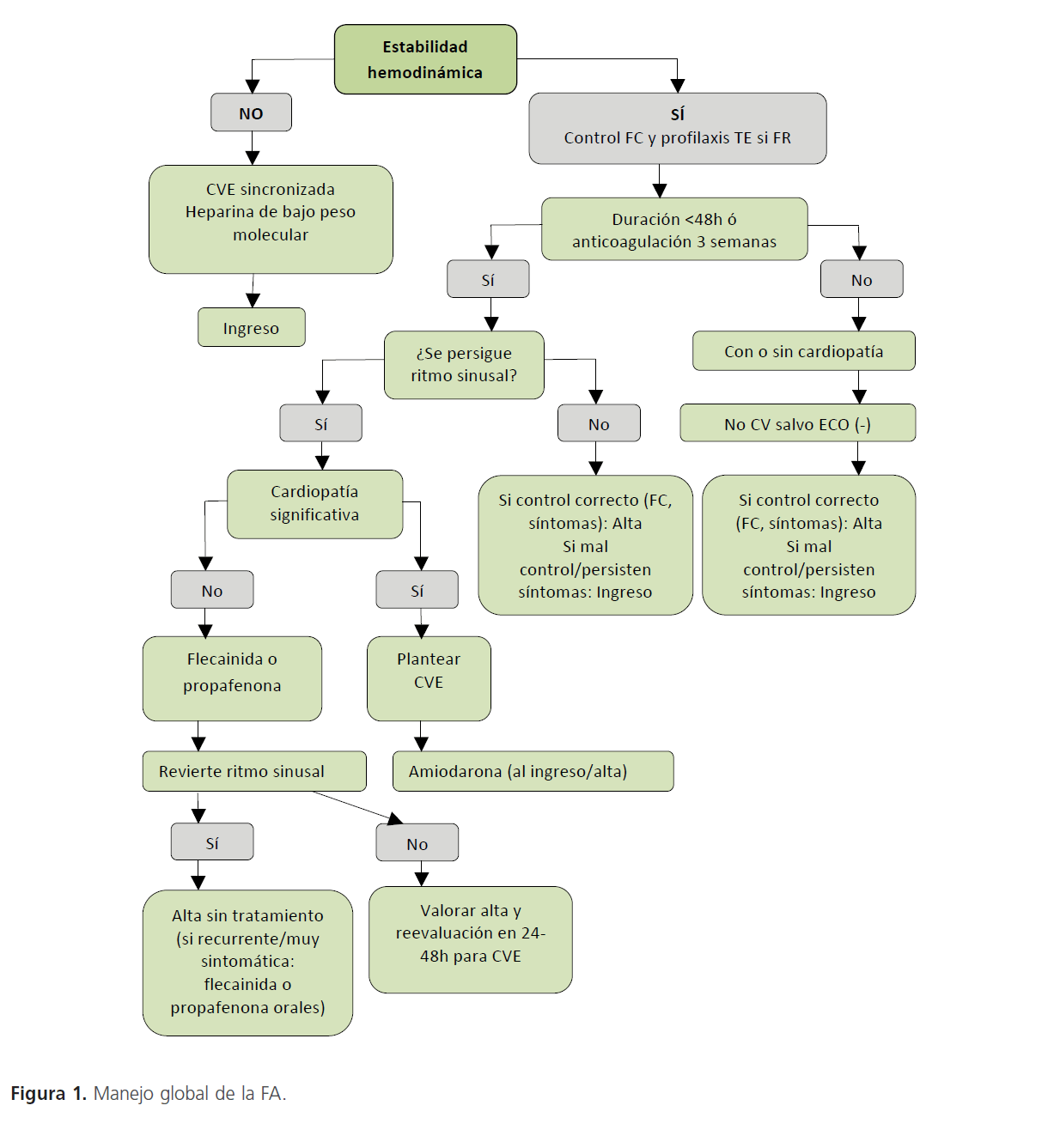
Figura 1: Manejo global de la FA.
B) Cardioversión eléctrica (CVE)
Programada: en pacientes con FA de más de 48 h de evolución o de comienzo incierto con ecocardiograma transesofágico normal o con ACO previa de al menos 4 semanas (se mantendrá posteriormente otras 3-4 semanas).
Urgente: reservada para situaciones de inestabilidad hemodinámica. En los casos en que la duración del episodio sea inferior a 48 h, se administrará una dosis previa de heparina (preferentemente heparina de bajo peso molecular) no siendo necesario continuar con la anticoagulación después de la cardioversión en pacientes sin factores de riesgo tromboembólico. Si existe riesgo de ACV se iniciará tratamiento anticoagulante de por vida. En pacientes con FA de más de 48 h de evolución e inestabilidad hemodinámica, es necesario sedar al paciente, cardiovertir eléctricamente y mantener el tratamiento anticoagulante durante al menos 4 semanas después de la cardioversión (I,B) tanto en la electiva como de urgencia. En los pacientes con factores de riesgo de ACV o recurrencia de la FA, el tratamiento anticoagulante (AVKs o NACOs) debe continuar durante toda la vida, independientemente del mantenimiento del ritmo sinusal tras la cardioversión [1] (I,B). La anticoagulación previa y posterior a una cardioversión se realiza con heparina, AVKs y NACOs (dabigatrán, todavía no se dispone de evidencia con rivaroxabán y apixabán aunque existen estudios en marcha) (I,B). Hay controversia sobre si poner tratamiento antiarrítmico post-CVE y cuánto tiempo mantenerlo.
C) Ablación con catéter de la aurícula izquierda
Dispone de gran eficacia en pacientes jóvenes y en las fases iniciales de la patología y se utiliza para aislar las venas pulmonares del resto de la aurícula, de esta forma, la FA que se produce dentro de estas venas queda recluida y no altera el normal funcionamiento del corazón.
La indicación principal es en pacientes con episodios de FA de origen focal, con existencia de mucha actividad eléctrica monotópica, en forma de extrasístoles auriculares muy frecuentes de la misma morfología y rachas de taquicardia o FA. En estos pacientes las tasa de mantenimiento del ritmo sinusal oscila entre 60-85%. Los resultados inmediatos y a medio plazo de la ablación de la FA en pacientes con FA persistente son ligeramente peores que los observados en FA paroxística, con tasas de éxito en torno al 60%.
Las complicaciones más frecuentes se relacionan con la maniobra de punción y, en este sentido, más allá de su carácter benigno y posible de resolución, están vinculadas con la experiencia del operador [21].
Los fármacos antiarrítmicos también se usan para el mantenimiento del ritmo sinusal una vez que se ha resuelto la FA de manera espontánea o por cardioversión eléctrica o farmacológica. Pueden retrasar la recaída en FA tras cardioversión.
Control de la frecuencia
El control de la FC es siempre un objetivo terapéutico en la FA para aliviar los síntomas, impedir el deterioro hemodinámico y evitar la aparición de taquimiocardiopatía e insuficiencia cardíaca [3]. En pacientes sin sintomatología, no se ha asociado con una mayor morbimortalidad [22]. El objetivo es mantener la FC entre 60-80 lpm en reposo y 90-115 lpm durante la actividad física moderada. Recientemente, se ha probado, que un control menos estricto es igual de beneficioso para el paciente en términos de supervivencia y calidad de vida, y es más fácil de conseguir [23]. Si el paciente persiste sintomático, se intentará un control estricto de la FC (<80 lpm en reposo y <110 lpm tras ejercicio moderado). Sin embargo, en pacientes con <80 lpm, se presentan más efectos secundarios y mayor índice de ingreso e implantación de marcapasos [24]. La elección del tratamiento farmacológico debe hacerse de forma individualizada. Los fármacos más utilizados son: betabloqueantes (preferiblemente cardioselectivos), antagonistas del calcio no dihidropiridínicos, digoxina y amiodarona (en controversia actualmente). Los betabloqueantes son los fármacos de elección mientras que los antagonistas del calcio no dihidropiridínicos son la alternativa en pacientes con clínica respiratoria (broncoespasmo sobre todo), cuando están contraindicados los anteriores (I,A). La digoxina, se reserva para el control de la FC en situaciones agudas con IC y para pacientes con movilidad reducida con intolerancia a los fármacos anteriores, aunque sería de elección en casos de terapia combinada (I,B). La amiodarona queda restringida a las formas permanentes. En caso de fracaso terapéutico y de manera individualizada, se puede plantear ablación del nodo auriculoventricular o implantes cardíacos (marcapasos, terapia de resincronización, desfibrilador). Se considera indicada la terapia de resincronización cardiaca en pacientes a los que se realiza ablación del nodo auriculoventricular por FA persistente y se encuentran en clase funcional II-III de la NYHA con disfunción ventricular significativa. Sin embargo, es escasa la evidencia sobre el beneficio de dicha terapia en pacientes con disfunción ventricular, insuficiencia cardiaca avanzada y FA sin ablación del nodo auriculoventricular. Consideramos implantación de marcapasos (preferentemente en modo DDD o AAI) en aquellos pacientes con indicación de estimulación cardíaca por bradicardia (FA lenta) y en aquellos a los que se les practicó ablación del nodo aurculoventricular. Diversos estudios han demostrado que el desfibrilador auricular puede ser empleado de forma ambulatoria para tratar de forma eficaz y segura episodios de FA. Se ha demostrado que el dispositivo puede detectar correctamente los episodios de FA con una especificidad del 100%, una sensibilidad del 92,3% y un valor predictivo positivo del 97,4% para la diferenciación de ritmo sinusal. Además todos los choques fueron correctamente sincronizados con la onda R, sin producirse ninguna proarritmia [21].
El control de la FC es la opción adecuada en FA permanente; siendo necesario asociar tratamiento antitrombótico/anticoagulante.
Tratamiento farmacológico en la fibrilación auricular
A) Betabloqueantes
Están indicados en el control de la FC, tanto en reposo como en ejercicio en pacientes con cualquier tipo de FA (I,C) y en IC. Los fármacos recomendados son los cardioselectivos: carvedilol, metoprolol y bisoprolol. No se recomienda el manejo de sotalol con el único objetivo de controlar la FC por el riesgo de arritmias ventriculares; sin embargo, es efectivo en el mantenimiento del ritmo sinusal tras la cardioversión. Han de usarse con precaución en pacientes asmáticos y con EPOC. Su retirada ha de ser gradual pues presentan efecto rebote (Figura 2).
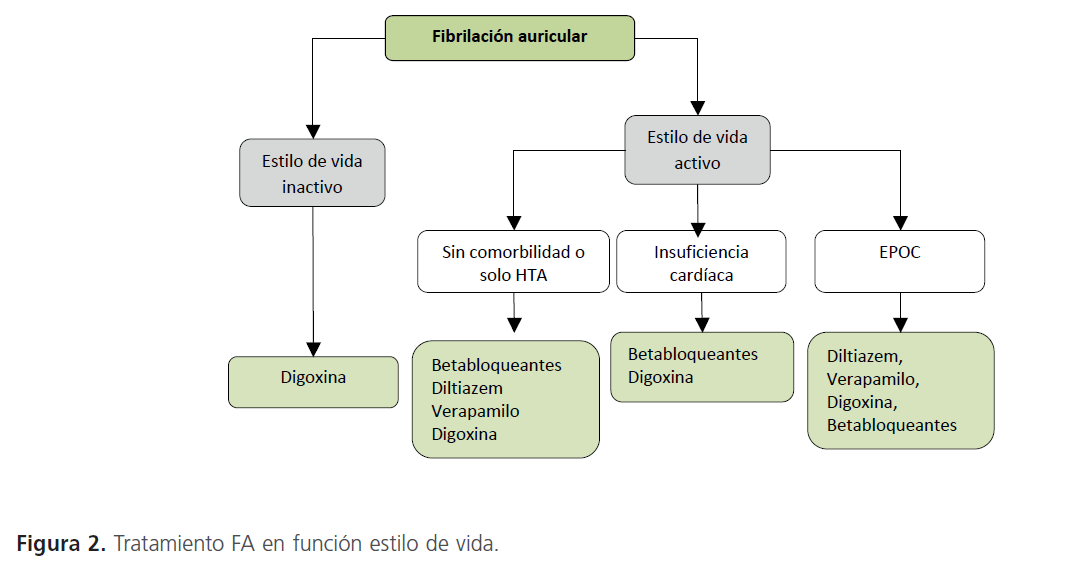
Figura 2: Tratamiento FA en función estilo de vida.
B) Antagonistas del calcio
Constituyen la segunda alternativa terapéutica en el tratamiento de la FA, cuando los anteriores están contraindicados; controlan la FC tanto en reposo como durante el ejercicio, aunque tienen el inconveniente de su efecto inotrópico negativo. Se usan los antagonistas del calcio no dihidropiridínicos que tienen efecto antiarrítmico: diltiazem y verapamilo.
C) Digoxina
Es la tercera alternativa en el control de la FC y no es mejor que placebo en el control del ritmo. No se utiliza como agente único para controlar la respuesta ventricular en pacientes con FA paroxística [3]. A diferencia de los anteriores, sólo controla la FC en reposo. Presenta efecto inotrópico positivo con lo que su efecto es más lento. Es un fármaco con estrecho margen terapéutico lo que implica necesidad de monitorizar niveles plasmáticos. Es necesario tener precauciones en pacientes con afectación renal.
D) Amiodarona
Es un fármaco de elección en la cardioversión farmacológica, sobre todo cuando existe cardiopatía [3]. Presenta elevada vida media; el efecto puede durar hasta un mes después de suspender el tratamiento. Su inconveniente son los efectos adversos (fototoxicidad, disfunción tiroidea, alteraciones hepáticas…) y el efecto bradicardizante. Se reserva para pacientes con enfermedad coronaria, disfunción sistólica moderada/ severa o hipertensión con hipertrofia significativa del ventrículo izquierdo.
E) Dronedarona
Es un fármaco antiarrítmico, similar a la amiodarona, aunque con menor toxicidad y vida media más corta (24 horas aproximadamente). Está indicada en el mantenimiento del ritmo sinusal en pacientes con FA y flutter auricular que han revertido de manera espontánea o tras cardioversión programada. No es útil en la cardioversión farmacológica. Disminuye la necesidad de hospitalización por eventos cardiovasculares en FA paroxística y tras la conversión de FA persistente. No debe ser administrada cuando la función ventricular está deprimida, tras una descompensación de insuficiencia cardíaca, ni en la insuficiencia cardíaca de clase funcional IV (Tabla 11), siendo de elección en estos casos amiodarona.
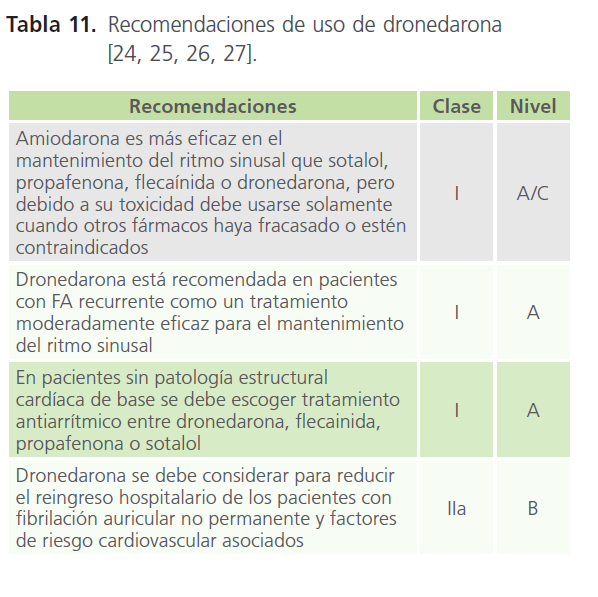
Tabla 11: Recomendaciones de uso de dronedarona [24, 25, 26, 27].
F) Otros antiarrítmicos
La flecainida y la propafenona están contraindicadas en cardiopatía isquémica por riesgo de desencadenar arritmias graves. Si no existe enfermedad estructural del corazón se recomienda: flecainida, dofetilida, propafenona o ibutilida [3].
G) Estatinas
El uso de estatinas se asocia con la disminución de episodios de FA tras cirugía cardíaca o síndrome coronario agudo. Se debe considerar el uso de estatinas después de la cirugía de by-pass aislada o asociada a intervenciones valvulares, cuando existe una cardiopatía subyacente, sobre todo, IC (IIb,B) como prevención primaria.
H) Inhibidores de la enzima convertidora de angiotensina (IECA) y antagonistas de los receptores de angiotensina (ARA II)
Los estudios realizados con ARA II muestran que estos fármacos tienen un papel en la prevención primaria de los episodios iniciales o recurrentes de la FA asociados a HTA, DM, IC o infarto de miocardio [3] (IIa, B).
No está considerado el tratamiento con IECAs y ARA II como prevención primaria de la FA en pacientes sin enfermedad cardiovascular aunque no existe todavía indicación formal para prescribirlos en FA con esta finalidad (III, C).
En prevención secundaria, es necesario considerar pre-tratamiento con IECAs y ARA II en pacientes con FA recurrente y que estén recibiendo tratamiento antiarrítmico (IIb, B). Los IECAs y los ARA II pueden ser útiles para la prevención de la FA paroxística o en pacientes con FA persistente que se someten a cardioversión eléctrica en ausencia de cardiopatía estructural significativa, cuando estos fármacos están indicados por otras razones (IIb, B).
Recomendaciones de tratamiento antiarrítmico en función de la duración de la fibrilación auricular
A) Primer episodio de FA
Es difícil determinar cuándo es el primer episodio de FA, especialmente cuando ésta es asintomática. Si el problema se soluciona espontáneamente no es necesario prevenir las recurrencias con tratamiento farmacológico; sólo se tendrá en cuenta en pacientes muy sintomáticos. En caso de existir factores de riesgo de tromboembolismo será preciso iniciar tratamiento anticoagulante excepto si se identifica un factor reversible precipitante de la FA [3] (Figura 3).
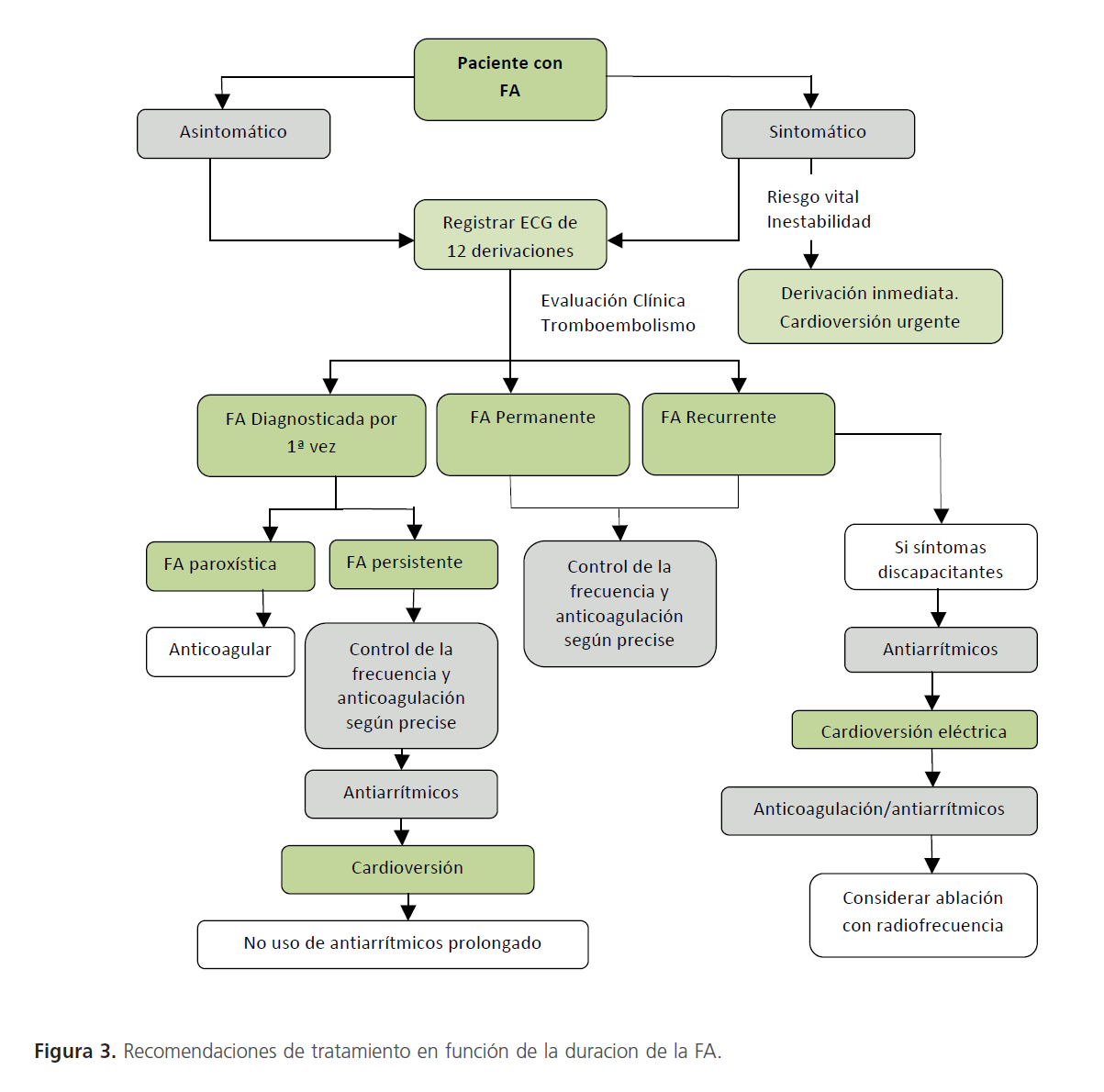
Figura 3: Reco mendaciones de tratamiento en función de la duracion de la FA.
B) FA paroxística
Suele desaparecer de forma espontánea en 24-48 horas cuando está relacionada con un factor desencadenante y se trata el mismo, aunque en muchos casos no existe un desencadenante concreto.
Los casos sintomáticos (con o habitualmente sin enfermedad estructural cardíaca o coronaria) se tratan con betabloqueantes. Si existe cardiopatía estructural (inusual en este tipo de FA) y no han sido eficaces los fármacos anteriores se recomienda el uso de amiodarona.
Existe la alternativa en pacientes seleccionados, con pocos episodios de FA paroxística y sin cardiopatía de base, usar un antiarrítmico autoadministrado en el momento de la crisis (estrategia de “pill in the pocket”) con el fin de frenar precozmente la aparición de los paroxismos y restablecer y mantener el ritmo sinusal. Los fármacos estudiados en cuanto a eficacia, seguridad y minimización de efectos proarrítmicos son flecainida, propafenona y sotalol [3].
La decisión del tratamiento antitrombótico en la FA paroxística está basada en los criterios de estratificación de riesgo, como una FA permanente.
C) FA persistente
El objetivo de tratamiento de la FA persistente estará basado en el control del ritmo o de la FC. Ambas opciones de tratamiento no se consideran excluyentes. Es preciso realizar una valoración individualizada en base a la opinión del paciente, la presencia de síntomas asociados a la arritmia y patologías concomitantes.
La FA revierte con éxito si desaparece la causa precipitante (fiebre, infección respiratoria) no siendo necesario administrar tratamiento farmacológico. Si el factor precipitante no se identifica o no existe enfermedad cardíaca estructural se inicia tratamiento con betabloqueantes u otros antiarrítmicos. Cuando éstos no son efectivos, tolerados o están contraindicados, el fármaco de elección es amiodarona [27]. Si a pesar de las recomendaciones previas el paciente permanece sintomático o no ha tolerado el tratamiento se considerarán otras medidas terapéuticas no farmacológicas como la ablación con catéter de la aurícula izquierda (de elección), la ablación del nodo AV y marcapasos o la ablación quirúrgica, que presenta peores resultados que las técnicas de ablación percutánea [3]. El uso de antiarrítmicos obliga a la anticoagulación para evitar el riesgo de embolia de la cardioversión. Si se decide utilizar fármacos para el control de la FC se actuará como en la FA permanente.
D) FA permanente
El objetivo de tratamiento de la FA permanente es el control de la FC mediante fármacos betabloqueantes o antagonistas del calcio no dihidropiridínicos en monoterapia. Como alternativa, en pacientes con vida sedentaria, se usa digoxina en monoterapia. Cuando ésta es insuficiente y es preciso controlar la FC (sólo durante las actividades diarias) es preciso combinar digoxina junto con betabloqueantes o antagonistas del calcio. Si no se consigue controlar la FC con tratamiento farmacológico o se sospecha de una miocardiopatía mediada por taquicardia se planteará la ablación por catéter del nodo AV e implante de marcapasos [3].
638
References
- Fuster, V., Rydén, LE., Cannom, DS., Crijns, HJ., Curtis, AB., Ellenbogen, KA. et al. ACC/AHA/ESC 2006 Guidelines for the Management of Patients with Atrial Fibrillation: A report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Revise the 2001 Guidelines for the Management of Patients With Atrial Fibrillation): Developed in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society. Circulation 2006; 114 (7): e257-e354.
- Camm, AJ., Lyp, GY., De Caterina, R., Savelieva, I., Atar, D., Hohnloser, SH. et al. 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: an update of the 2010 ESC Guidelines for the management of atrial fibrillation. Developed with the special contribution of the European Heart Rhythm Association. Eur Heart J. 2012; 33 (21): 2719-47.
- Camm, AJ., Kirchhf, P., Lyp, GY., Schotten, U., Savelieva, I., Ernst, S. et al. European Heart Rhythm Association. European Association for CardioThoracic Surgery Guidelines for the management of atrial fibrillation. The Task Force for the Management of Atrial Fibrillation of the European Socety of Cardiology (ESC), European Heart Journal 2010; 31: 2369-429.
- Furie, KL., Kasner, SE., Adams, RJ. et al. Guidelines for the Prevention of Stroke in Patients With Stroke or Transient Ischemic Attack: A Guideline for Healthcare Professionals From the American Heart Association/American Stroke Association. Stroke 2011; 42: 227-76.
- Furberg, CD., Psaty, BM., Manolio, TA., Gardin, JM., Smith, VE., Rautaharju, PM. Prevalence of atrial fibrillation in elderly subjects (the cardiovascular health study). Am J Cardiol. 1994; 74: 236-41.
- Kannel, WB., Benjamin, EJ. Epidemiology of atrial fibrillation. Med Clin North Am. 2008; 92: 17.
- LĂ³pez Castro, J., AlmazĂ¡n Ortega, R., PĂ©rez Romero, M., GonzĂ¡lez Juanatey, JR. Mortality prognosis factors in heart failure in a cohort of North-West Spain. EPICOUR study. Rev Clin Esp. 2010; 210 (9): 438- 47.
- Cheng, A., Kapil, K. Overview of atrial fibrillation. UptoDate version 19.2. [Internet]. Walthman (MA): UpToDate; 2011. Disponible en: https://www.uptodate.com.
- Kirchhof, P., Auricchio, A., Bax, J., Crijns, H., Camm, J., Diener, HC. et al. Ourcome parameters for trials in atrial fibrillation: executive summary. Recomendations from a consensus conference organized by the German Atrial Fbrillation Competence Network (AFNET) and the European Heart Rhythm Association (EHRA). Eur Heart J. 2007; 28: 2803-17.
- Pisters, R., Lane, DA., Nieuwlaat, R. et al. A novel user-friendly score (HAS-BLED) to assess 1-year risk of major bleeding in patients with atrial fibrillation: the Euro Heart Survey. Chest 2010; 138: 1093-1100.
- Dentali, F., Douketis, JD., Lim, W., Crowther, M. Combined aspirin-oral anticoagulant therapy compared with oral anticoagulant therapy alone among patients at risk for cardiovascular disease: a meta-analysis of randomized trials. Arch Intern Med. 2007; 167 (2): 117-24.
- Manning, WJ., Singer, DE., Lip, GYH. Antithrombotic therapy to prevent embolization in nonvalvular atrial fibrillation. UptoDate version 19.2. [Internet]. Walthman (MA): UpToDate; 2011. Disponible en: https://www.uptodate.com.
- Eriksson, BI., Quinlan, DJ., Eikelboom, JW. Novel oral factor Xa and thrombin inhibitors in the management of thromboembolism. Annu Rev Med. 2011; 62: 41-57.
- OrdovĂ¡s Baines, JP., Climent Grana, E., Jover Botella, A., Valero GarcĂa, I. Pharmacokinetics and pharmacodynamics of new oral anticoagulants. Farm Hosp. 2009; 33: 125-33.
- Escobar, C., Barrios, V., Jiménez, D. Atrial fibrillation and dabigatran: has the time come to use new anticoagulants? Cardiovasc Ther. 2010; 28: 295-301.
- Cid-Conde, L., LĂ³pez-Castro, J. New oral anticoagulants in Atrial Fibrillation. Atrial Fibrillation-Mechanisms and treatment. Croatia, 2013. https://dx.doi.org/10.5772/53614.
- Connolly, SJ., Pogue, J., Eikelboom, I. et al. ACTIVE W Investigators. Benefit of oral anticoagulant over antiplatelet therapy in atrial fibrillation depends on the quality of international normalized ratio control achieved by centers and countries as measured by time in therapeutic range. Circulation 2008; 118: 2029-37.
- Chung, MK., Shemanski, L., Sherman, DG., Greene, HL., Hogan, DB., Kellen, JC. et al. AFFIRM Investigators. Functional status in rate-versus rhythm-control strategies for atrial fibrillation: results of the Atrial Fibrillation Follow-Up Investigation of Rhythm Management (AFFIRM) Functional Status Substudy. J Am Coll Cardiol. 2005; 46 (10): 1891-9.
- Roy, D., Talajic, M., Nattel, S., Wyse, DG., Dorian, P., Lee, KL. et al. Rhythm control versus rate control for atrial fibrillation and heart failure. N Engl J Med. 2008; 258: 2667-77.
- Lip, GY., Watson, T. Atrial fibrillation (acute onset). Online. Clin Evid 2008.
- Calkins, H., Reynolds, MR., Spector, P., Sondhi, M., Xu, Y., Martin, A. et al. Treatment of atrial fibrillation with antiarrhythmic drugs or radiofrequency ablation: two systematic literatura reviews and metaannalyses. Cic Arrhythm Electrophysiol. 2009; 2: 349-61.
- Van Gelder, IC., Groenveld, HF., Crijns, HJ., Tuininga, YS., Tijssen, JG., Alings, AM. et al. Lennient versus strict rate control in patients with atrial fibrillation. N Eng J Med. 2010; 362: 1363-73.
- Wyse, DG., Waldo, AL., DiMarco, JP., Domanski, MJ., Rosenberg, Y., Scron, EB. et al. Atrial fibrillation follow-up investigation of rhythm management (AFFIRM) investigators. A comparison of rate control and rhythm control in patients with atrial fibrillation. N Engl J Med. 2002; 347: 1825.
- Hohnloser, SH., Crijns, HJ., van Eickels, M., Gaudin, C., Page, RL., Torp- Pedersen, C., Connolly, SJ. Effect of dronedarone on cardiovascular events in atrial fibrillation. N Engl J Med. 2009; 360: 668-678.
- Singh, BN., Connolly, SJ., Crijns, HJ., Roy, D., Kowey, PR., Capucci, A., Radzik, D., Aliot, EM., Hohnloser, SH. Dronedarone for maintenance of sinus rhythm in atrial fibrillation or flutter. N Engl J Med. 2007; 357: 987-29.
- Davy, JM., Herold, M., Hoglund, C., Timmermans, A., Alings, A., Radzik, D., Van Kempen, L. Dronedarone for the control of ventricular rate in permanent atrial fibrillation: the Efficacy and safety of dRonedArone for the cOntrol of ventricular rate during atrial fibrillation (ERATO) study. Am Heart J. 2008; 156: 527.e1-527.e9.
- Lafuente-Lafuente, C., Mouly, S., Longas-Tejero, MA., Bergmann, JF. Antiarrhythmics for maintaining sinus rhythm after cardioversion of atrial fibrillation. Cochrane Database Syst Rev. 2007; 4: CD005049.
- Wann, LS., Curtis, AB., Ellenbogen, KA., Estes, NA., Ezekowitz, MD., Jackman, WM. et al. 2011 ACCF/AHA/HRS focused update on the management of patients with atrial fibrillation (update on dabigatran): a report of the American College of Cardiology Foundation/American Heart Association Task Force on practice guidelines. J Am Coll Cardiol. 2011; 57 (11): 1330-7.



















