Investigating Article - (2023) Volume 19, Issue 1
Necrosis De Cabeza Femoral: EtiologÃa, Clasificación Y Tratamiento: Revisión Bibliográfica
Claudia Lidueña1*,
Alejandro Mendoza1,
Andrés Malo2 and
Adel Al Awad3
1CEDIAH: Comunidad Estudiantil para la Difusión e Investigación de la Anatomía Humana, Escuela de Medicina, Universidad del Zulia (LUZ), Venezuela
2Médico general del Hospital San Francisco de Asís, Colombia
3Cirujano Hepatobilio pancreático en
torre promotora en Clínica Paraíso de
Maracaibo, Venezuela
*Correspondence:
Claudia Lidueña,
CEDIAH: Comunidad Estudiantil para la Difusión e Investigación de la Anatomía Humana, Escuela de Medicina, Universidad del Zulia (LUZ),
Venezuela,
Email:
Received: 03-Jan-2023, Manuscript No. ipadm-23-13439;
Editor assigned: 05-Jan-2023, Pre QC No. ipadm-23-13439;
Reviewed: 19-Jan-2023, QC No. ipadm-23-13439;
Revised: 21-Jan-2023, Manuscript No. ipadm-23-13439;
Published:
28-Jan-2023, DOI: 10.36648/1698-9465.23.19.1579
Abstract
Femoral Head Necrosis (FNC) or osteonecrosis is a pathological process that leads to bone cell death, as a result of a temporary reduction or complete loss of blood supply; It is difficult to establish the relationship of a true cause of NCF due to the low prevalence of some etiologies. The objective of this research was to determine the appropriate diagnostic method for SCN by reviewing the literature. For NCF, the first diagnostic classification used was described by Ficat and Arlet; based on radiographic findings in the anteroposterior and axial planes, it consisted of 4 stages (I, II, III, IV), being easy and simple, however, there are controversies because magnetic resonance imaging (MRI) is not incorporated. There is another Steinberg classification based on the previous one; it presents 7 stages, using the 2 radiographic planes, bone scintigraphy and MR images for disease staging. , the ARCO classification was described, this unites the ficat and arlet models with steinberg, subsequently incorporating radiographs, computed tomography, MR and scintigraphy to locate the size and location of the necrotic area, adapting the Sugano classification, based on NMR, to this method useful to prevent collapse of the femoral head when lesions do not yet appear on plain radiographic examination. This research concluded that the appropriate diagnostic method for NCF corresponds to the ARCO classification due to the incorporation of various diagnostic images that will adopt the best treatment according to the pathology stay. The treatment of NCF can be conservative with drugs or through surgical management depending on the stage of involvement; osteotomy being its objective to remove necrotic tissue from weight-bearing areas or hip arthroplasty being the procedure of choice when treating large collapsed lesions.
Keywords
Femur, Necrosis, Osteonecrosis.
INTRODUCTION
La Necrosis en Cabeza Femoral (NCF), también conocida como
osteonecrosis, es un proceso patológico que conduce a la
muerte de los elementos celulares del hueso, como resultado
de una reducción temporal o perdida completa de suministro de
sangre [1-16]. El caso de la cabeza femoral es la localización más
común de la necrosis avascular, responsable 3% de las coxopatias
del adulto, producto de la disminución del flujo sanguíneo en el
segmento afectado del hueso produciendo muerte de los osteocitos
y la medula ósea que lleva al desgaste articular, desencadena en
el colapso de la articulación, provocando dolor y limitación para la
movilidad [3]. La condición es progresiva y debilitante que puede
resultar en un aumento significativo de la morbilidad de los pacientes
que la padecen en cualquier edad [17-22].
En general, esta afección es más frecuente en hombres que
en mujeres, y los estudios estiman las relaciones de 3:1 a 5:1
respectivamente. Los pacientes que presentan dicha patología
son principalmente adultos, se ubican entre los 30 y 60 años de
edad, aunque puede afectar a hombres y mujeres de cualquier
edad; hay aproximadamente 10.000 a 20.000 nuevos casos
reportados cada año solo en los Estados Unidos, lo que contribuye
al 10% de las aproximadamente 250.000 artroplastias totales de
cadera realizadas anualmente y existen entre 300 mil y 600 mil
personas en el mundo que padecen esta condición. [3,8,1].
La NCF es una patología progresiva que conlleva al colapso de
la articulación, por ende, es limitante, y cada vez se presenta
en aumento; El objetivo de la revisión es describir la manera
más eficaz para su diagnóstico temprano y su estadificación y
prevenir el reemplazo de la porción afectada del hueso que es el
tratamiento final ante un diagnóstico tardío.
Estrategias Metodológicas
Se efectuó un análisis narrativo a través de diferentes bases de
datos, tales como ScienceDirect, Scielo, PubMed, entre otras.
la exploración y selección de artículos fue realizada en revistas
indexadas en idioma inglés a partir desde el año 2014 hasta el 2023. Según la metodología DeCS y MeSH para la selección
de palabras claves se utilizaron los términos: Fémur; Necrosis;
osteonecrosis. Reconocimos 80 publicaciones asociadas con la
temática, de estos, 25 artículos cumplieron con los requisitos de
inclusión, tales como, artículos no menores al año 2014, artículos
de texto completo y que informaran sobre necrosis de cabeza
femoral. Entre la exclusión se tuvo en cuenta que los artículos
no contaran con suficiente información y que no presentaran el
texto completo al momento de su revisión.
Resultados
Etiología
Varios estudios acerca las causas de osteonecrosis de cabeza femoral
concuerdan en los mecanismos fisiopatológicos involucrados en su
aparición, los cuales generalmente inician luego de 2 a 3 horas de
hipoxia celular con la muerte de los osteocitos, posteriormente se
torna hiperémica y se inicia un proceso de angiogénesis en el área
adyacente de la lesión con fines de reparación, reabsorbiendo tejido
óseo muerto y reemplazándolo por nuevo hueso vivo; sin embargo
el proceso de resorción supera el de formación produciendo perdida
de integridad estructural de la trabécula, fractura subcondral y
colapso articular [12,17].
Ha sido difícil establecer la relación de que un factor de riesgo
determinado constituya una verdadera causa de NCF debido a
la baja prevalencia de algunas etiologías, reportándose como
idiopática en algunos estudios [17]. Esto ha llevado a que
se clasifiquen en dos grupos a los pacientes que la padecen,
aquellos sin aparente etiología definida o factor de riesgo, y los
que tienen una etiología claramente establecida. Para establecer
esta etiología se hace necesario subdividir el mecanismo que
lleva a esta condición en traumático y no traumático, así como
puede resultar de la combinación de ambos factores [3]
En la osteonecrosis (ON) secundaria a trauma los vasos sanguíneos
alrededor de la cabeza femoral sufren daño directo por la lesión,
que usualmente se trata de fractura intracapsular de la cabeza
femoral en un 15% a 50%, o a dislocación de la cadera en el 15% a 25% de los casos [3,12,15,17]. En el caso de las osteonecrosis
atraumáticas, se han identificado factores genéticos, metabólicos,
y locales que afectan el suministro de sangre al hueso. Se ha
asociado el uso de altas dosis de corticoides sistémicos en un 35%-
40%, y el consumo excesivo de alcohol en 20%-40% al desarrollo
de osteonecrosis, presentando alteraciones en la circulación de
lípidos, que llevan a la formación de microtrombos que afectan la
circulación del hueso [9,12,14,15].
La oclusión vascular puede ocurrir secundaria a patologías
que aumenten la coagulación intravascular y formación de
trombos, como anticuerpos antifosfolipidos, trombofilia, e
hipofibrinolisis [4]. También pueden desencadenar el proceso
oclusivo condiciones hematológicas como la anemia falciforme,
o acumulación de células la medula ósea como en la enfermedad
de Gaucher. Todas estas causas no traumáticas se relacionan
principalmente con población joven, y hasta un 80% con el uso
de alcohol y corticoides [6,9,12,14,15].
Clasificación de Necrosis de Cabeza de Fémur
Clasificación de Ficat y Arlet
Fue la primera clasificación utilizada para la NCF descrita en los
años 60 por Ficat y Arlet. Primordialmente esta clasificación
basada en los hallazgos radiográficos en los planos anteroposterior
y axial constaba de 4 estadios (I, II, III, IV), luego en 1985 sufrió
una modificación agregándole el estadio “0” [18].
• Estadio 0: representa un estado prepatológico sin signos
clínicos ni radiograficos.
• Estadio I: es definido como una apariencia radiográfica
normal de la cabeza de fémur. Puede existir señales de
edema con incremento de la medula ósea observados en RM
o aumento de marcador en la gammagrafía ósea.
• Estadio II: caracterizado por una apariencia de esclerosis
difusa y quistes de reparación ósea
• Estadio III: es caracterizado por fractura subcondral a veces
puede parecer una cresta cerca de la superficie articular, esto
se conoce como “signo de la cresta” que es patognomico
de esta patología. El colapso es evidente y el aplanamiento
puede comenzar a surgir.
• Estadio IV: en este estadio se evidencia un mayor colapso
de la articulación, aplanamiento y destrucción de la cabeza
de fémur. Secundario a esto se incluye aplanamiento del
espacio, restauración ósea y quistes óseos subcondrales.
Esta una clasificación es fácil y simple para ponerla en práctica,
pero existen diversas controversias debido a que no está
incorporado el estudio por resonancia magnética. Sumado a
esto también hay controversias en las caderas que presentan
el signo de la cresta sin aplanamiento condral deben agruparse
con aquellas que presentaron un aplanamiento importante de la
cabeza femoral [18].
Clasificación de Steinberg
Esta es otra clasificación basada en la descrita por Ficat y Arlet.
Presenta 7 estadios, utilizando los 2 planos radiograficos,
gammagrafía ósea y principalmente imágenes de RM para la
estadificación de la enfermedad tomando en cuenta el tamaño
de la lesión, morfología y cambios claros de la cabeza femoral.
Cabe resaltar que este sistema de estadificación es más detallado
que el de Ficat y Arlet debido a que incorpora el tamaño de la
lesión [18] [Tabla 1].
| Stage |
Findings |
Techniques |
Subclassification |
Quantitation |
| 0 |
None |
Radiography , computed
tomography , scintigraphy .
magnetic resonance imaging |
No |
No |
| 1 |
Radiography and computed tomography
normal At least ONE of the other
techniques is positive |
Scintigraphy , magnetic
resonance imaging |
Location of lesion
Medial
Central .
Lateral |
Area of involvement ( percentage )
A : Minimal ( < 15 % )
B : Moderate ( 15 to 30 % )
C : Extensive
Length of crescent
A : < 15 %
B : 15 to 30 %
C : > 30 %
Surface collapse and dome depression
A : < 15 % and < 2 mm
B : 15 to 30 % and 2 to 4 mm
C : > 30 % and > 4 mm |
| 2 |
Sclerosis , osteolysis , focal osteoporosis |
Radiography , computed
tomography , scintigraphy
and magnetic resonance
imaging |
Same as stage 1 |
Same as stage 1 |
| 3 |
CRESCENT SIGN and / or flatening
of articular surface |
Radiography and computed
tomography |
Same as stage 1 |
Same as stage 1 |
| 4 |
Osteoarthritis , acetabular changes , joint |
Radiography only |
No |
No |
Tabla 1.Clasificación ARCO (Association Research Circulation Osseous).
• Estadio 0: ausente de síntomas clínicos y cambio
radiográficos.
• Estadio I: caracterizado por aparente normalidad radiográfica,
pero con cambios tempranos en RM o en gammagrafía ósea
de la enfermedad.
• Estadio II: se caracteriza por esclerosis difusa área esclerotica
o cambios quísticos en la cabeza femoral.
• Estadio III: es un estado de colapso temprano evidenciándose
el signo de la cresta sin aplanamiento de la cabeza femoral.
• Estadio IV: se evidencia lesiones asociadas con aplanamiento
de la cabeza femoral.
• Estadio V: muestra cambios acetabulares con aplanamiento
de la cabeza femoral, pero sin afectación acetabular.
• Estadio VI: evidenciado en casos avanzados de la enfermedad
con cambios en ambos lados de la articulación.
Clasificación ARCO (Association Research
Circulation Osseous)
Establecida en 1991 la estadificación ARCO une los modelos ficat
y arlet con steinberg, incorporando radiografías, tomografía
computarizada, RM y gammagrafía para localizar el tamaño y
ubicación del área necrótica. Este consta de 5 estadios (0-4) e
incorpora subclasificaciones teniendo en cuenta la localización
de la lesión [18].
Ha sufrido diversas modificaciones y ausencia de consensos para
terminar de formar una estadificación mas certera. Pero en un
consenso realizado en el 2019 se concluyó que; 1) eliminación
del estadio, 2) el estadio 3 es dividió en una etapa temprana (3A)
y tardía (3B) de acuerdo a la profundidad de la depresión de la
cabeza femoral y 3) la subclasificación de la localización y tamaño
no está incorporada [21].
Clasificación del Comité de Investigación
Japones (CIJ)
Realizado por el ministerio de salud, labor y bienestar japones
(Japanese Ministry of Health, Labor and Welfare “JMHLW”),
utilizando RM para clasificar la ON basado en la localización
de la lesión necrótica. El principio único de la clasificación es la
localización de la lesión necrótica relacionado con la región de
soporte de peso acetabular, que es un importante factor para
determinar el pronóstico final. Dependiendo del tamaño y la
localización de la lesión determina un factor importante en el
pronóstico de la lesión, debido a que una lesión en el área del
soporte del peso puede progresar rápidamente a un colapso de
la articulación, en cambio, si es ubicada en un área de no soporte
de peso no progresaría a un colapso de la articulación hasta un
estadio avanzado [18].
Esta clasificación propone 3 estadios:
• En el estadio A: la lesión ocupa 1/3 o menos de la porción
de soporte.
• En el estadio B: la lesión ocupa 2/3 o menos de la porción
de soporte.
• En el estadio C: la lesión ocupa más de 2/3 de la porción de
soporte, comprende 2 subcategorías; estadio C1 la lesión no se extiende lateralmente y estadio C2 la lesión se extiende
lateralmente al borde acetabular.
Un estudio de 74 pacientes diagnosticadas con NCF, en el que
compararon 3 tipos de clasificación (Stainberg, Kerboul modificado
y el CIJ), teniendo como conclusión de que la clasificación CIJ
era la más confiable y efectiva al menos en etapas temprana
(estadios A), también que era el único sistema que se clasificaron
NCF en estado favorable y no progresaron a un colapso [19].
Pero cada uno de estos métodos tiene sus propios contras. 1)
Las mediciones volumétricas pueden ser demasiado complicadas
para el uso clínico de rutina. 2)Las medidas angulares pueden
verse influenciadas por la forma de la lesión y la distancia desde
la superficie articular. 3) La clasificación de la ubicación no evalúa
específicamente el tamaño de la lesión. Si se hace referencia a
la lesión de la cabeza femoral en relación con la superficie de
soporte de peso acetabular, puede verse influenciado por la
posición de la cadera durante el estudio de imagen [7].
Manifestaciones Clínicas
El dolor en la ingle es el síntoma de presentación, suele aparecer
en etapa tardía de la patología, seguido del dolor en muslos y
glúteos. Algunas veces se exacerba con la carga de peso y el
movimiento articular [15]. Sin embargo, puede presentarse
en reposo y en un tercio de los pacientes se presenta el dolor
nocturno. Los hallazgos físicos son en gran parte inespecíficos;
eventualmente, las limitaciones de movimiento se hacen
presente, particularmente con la rotación interna forzada y la
abducción [11].
En el examen clínico se debe prestar atención a la posible
presencia de una postura anormal o una cojera relacionada al
dolor o al acortamiento de las extremidades; En la NCF avanzada,
los hallazgos no difieren de los de coxartrosis primaria y puede
mostrar un patrón capsular con restricciones [2].
La NCF generalmente se aborda mediante [1]:
1) La revisión del historial médico del paciente.
2) La obtención de una evaluación radiológica adecuada.
3) La determinación del estadio de la afección.
4) El desarrollo de un plan para las opciones de tratamiento.
Diagnostico
Un estudio diagnóstico completo es particularmente importante
en las primeras etapas de la NCF atraumática. Los síntomas
inespecíficos y la ausencia inicial de anomalías en las radiografías
simples pueden llevar a un fatídico retraso en el diagnóstico y el
inicio del tratamiento. Junto con la historia clínica y el examen
físico, la imagen diagnóstica juega un papel importante [2].
Debido a que la mayoría de pacientes se presentan con un curso
tardío de la enfermedad, es necesario un alto índice de sospecha
cuando se atiende un paciente con factores de riesgo conocidos;
El diagnóstico temprano puede prevenir el colapso del hueso y la
posterior necesidad de un remplazo articular, Existen imágenes
relevantes para el diagnóstico son la radiografía simple,
tomografía computarizada (TC) y resonancia magnética (RM)
[15].
La radiografía constituye el método imagenológico más utilizado
[Figura 1] para detectar esta afección, sin embargo, es necesario
aclarar que en los estadios iniciales de la enfermedad es de poca
ayuda. Mediante el examen radiográfico puede realizarse la
clasificación adecuada en pacientes con NCF. Estas clasificaciones
radiográficas se dividen en 2 grandes grupos: cualitativas y
cuantitativas [1].
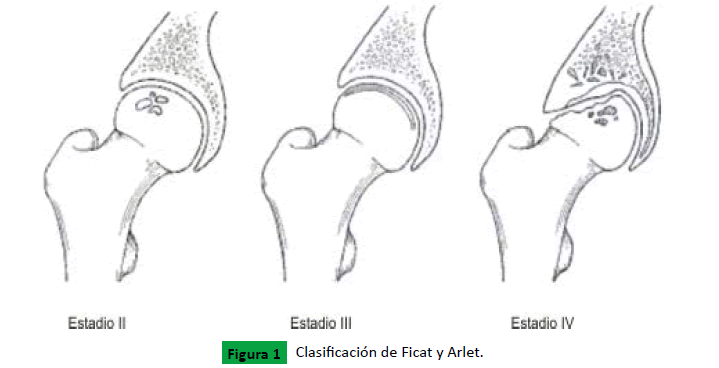
Figura 1. Clasificación de Ficat y Arlet.
La esclerosis y los cambios quísticos son cambios radiográficos
tempranos, mientras que la progresión de la enfermedad se
manifiesta con una pérdida de la esfericidad normal de la cabeza
femoral (colapso de la cabeza femoral por fractura subcondral) y
reducción del espacio articular y artritis secundaria [20].
La TC tiene mayor sensibilidad y especificidad que la radiografía
simple, pero también se dificulta visualizar la NCF temprana.
La TC de alta resolución con cortes de 1 a 2 mm permite una
muy buena demostración de las estructuras trabeculares, por lo
tanto, las fracturas subcondrales de importante pronóstico en la
fase temprana de inestabilidad mecánica, se visualizan mejor en
TC que en RM [2].
La RM es el estándar de oro, con más de 99% de especificidad y
sensibilidad al compararla con otros métodos de imagen, es la
herramienta de detección más útil en NCF temprana y para la
evaluación cuantitativa de la extensión de la enfermedad dentro
de la cabeza femoral [3,4]. La Resonancia Magnética Nuclear
(RMN) está considerada como el medio diagnóstico más efectivo para el diagnóstico de la osteonecrosis de cabeza femoral. Su
porcentaje de sensibilidad se encuentra entre 88 y 100 %, lo cual
cual es mucho más alto que el de la radiografía convencional, la
tomografía axial computarizada y la gammagrafía ósea. Además,
la RMN es muy útil para diferenciar la osteonecrosis de otras
enfermedades de la cadera [1].
Sugano22 propone otra clasificación basada en la RMN, muy útil
para prevenir el colapso de la cabeza femoral cuando aún no han
aparecido lesiones en el examen radiografico simple [1] [Tabla 2].
|
| Tipo |
Apariencia en la RMN . |
| I |
Presencia de línea de demarcación en la cabeza femoral .
IA La línea de demarcación más externa se localiza en el
tercio medio de la superficie de apoyo .
La línea de demarcación más externa se localiza en el
tercio central de la superficie de apoyo .
IC La línea de demarcación más externa se localiza en el
tercio lateral . |
| II |
Aplanamiento de la cabeza femoral en la superficie de
apoyo sin línea de demarcación . |
| III |
Lesiones radiolúcidas quísticas sin líneas de demarcación .
IIIA Lesiones quísticas localizadas anterior y medialmente
en la cabeza femoral , lejos de la zona de apoyo .
IIIB Lesiones quísticas localizadas en la zona lateral de la
superficie de apoyo . |
TABLA 2. Clasificación de Sugano.
Las imágenes juegan un papel importante para el diagnóstico
y determinación del estadio de la patología, pero sus
manifestaciones clínicas como lo es el dolor inguinal y de cadera
instalada por más de seis semanas que suele ser profundo e
intermitente, además que exacerba con movimiento y peso
pueden orientar a pesar que no van a dar un diagnóstico
definitivo.
Tratamiento
No hay un tratamiento universalmente establecido para la NCF
y es controversial en la literatura, sin embargo, existen metas
terapéuticas que se basan en conservar la articulación natural
tanto como sea posible de acuerdo con el estilo de vida de cada
paciente, edad, u ocupación. Luego de establecer el diagnóstico se
toman en cuenta diversos factores como la presencia de síntomas
crónicos, el tiempo de la lesión y su estado, determinando si hay o no colapso estructural y las comorbilidades del paciente, que
influyen en el tipo de manejo que se dará, pudiendo ser de forma
conservadora sin cirugía, o reemplazo articular cuando el colapso
estructural se encuentra en un estado avanzado [10].
Tratamiento No Quirúrgico
A pesar de la presencia de síntomas de dolor y limitación
funcional en los pacientes, el tratamiento inicial en la NCF suele
ser conservador. Con ello se busca lograr una disminución de
los síntomas secundarios a la afectación del cartílago y evitar el
progreso de la deformidad hacia la fractura subcondral y colapso
articular. Entre estos métodos encontramos la oxigenación en
cámara hiperbárica, cuyo objetivo es retrasar la evolución de la
enfermedad al aumentar la presión en el área necrótica logrando
reducir la activad osteoclástica, proliferación de los fibroblastos,
síntesis de colágeno y angiogénesis, mejorando a la vez la
microcirculación por estimular la vasoconstricción venosa [5].
En el manejo farmacológico de la ON se han postulado varias
teorías acerca de la fisiopatología de dicha enfermedad que
coinciden con la disminución e incluso interrupción de flujo
sanguíneo a la cabeza femoral. Por lo que se han estudiado
fármacos capaces de intervenir en este mecanismo tal como los
anticoagulantes, antihipertensivos y antihiperlipidemicos; o que
actúen evitando la pérdida de la integridad estructural del tejido
óseo como los bifosfonatos. Los AINEs y acetaminofén también
se usan para el alivio de los síntomas, así como algunos opioides,
sin embargo, estos últimos deben usarse con moderación y
periodos cortos de tiempo mientras se considera la posibilidad
del manejo quirúrgico [5,12].
Tratamiento Quirúrgico
El manejo quirúrgico se podría clasificar dependiendo del estadio
de afectación entre fase temprana y fase tardía. Y a la vez es
posible relacionarlos con los que conservan la cabeza femoral
necrótica cuyo uso principal se da en fases tempranas de la
enfermedad, y los que realizan reemplazo total de la articulación
que están reservados para las fases más avanzadas de colapso
articular [5,12].
Uno de los procedimientos más utilizados y de mayor eficacia
para fases tempranas es la descompresión de núcleo, cuya
finalidad es reducir la presión intramedular dentro de la cabeza
femoral para mejorar el dolor y la regeneración ósea. Es una
técnica mínimamente invasiva donde ser perfora de forma
percutánea la cabeza femoral para crear canales que mejoren
la microvascularización en la zona afectada Las tasas de éxito
varían ampliamente de 40% a 100% dependiendo del estado
del paciente, viendo resultados más satisfactorios al tratarse
en el estadio más temprano de la enfermedad. Muchos de los
pacientes con descompresión del núcleo exitoso pueden retomar
sin problemas a su antigua calidad luego de varios meses [12,13].
El injerto óseo
Consiste en la inserción de tejido óseo el cual es trasplantado
al área necrótica, lo cual proporciona soporte estructural y
puede funcionar como base para la formación de nuevo hueso
y evitar el colapso. Los injertos pueden ser no vascularizados
o vascularizados, estos últimos con la cualidad que mejoran la perfusión en las áreas isquémicas del hueso. Existen tres
técnicas que utilizan injertos óseos no vascularizados: Trapdoor,
Phemister y Lightbulb, siendo esta ultima la más utilizada, y la
indicación para llevarla a cabo es NCF en estadio de precolapso
o al menos en estadios tempranos poscolapsada la articulación,
con menos de 2 mm de colapso y superficie articular intacta [13].
Osteotomía
Su objetivo es remover el tejido necrótico del hueso de las
áreas de soporte de peso para redistribuir las fuerzas sobre la
articulación por medio de la rotación de la posición del cuello
del fémur y la cabeza. Aunque muchos estudios han reportado
resultados prometedores tiene una alta tasa de complicaciones,
puede empeorar la dificultad de una nueva intervención
quirúrgica tal como la artroplastia en un estadio final y reducir su
posterior efectividad, por lo cual no se ha estandarizado [13,5].
Artroplastia total de cadera
Es el único procedimiento de elección cuando se tratan lesiones
colapsadas de gran tamaño que pueda ofrecer un alivio
significativo a los síntomas y restaurar la funcionalidad de la
articulación. Consiste en reemplazar la cabeza femoral afectada
por una prótesis artificial hecha de metal y plástico, al tiempo
que se reemplaza la superficie articular del acetábulo para que
no se desgaste de forma acelerada por la prótesis. Tienen una
vida media de unos 15 años antes de que presenten desgaste y
que requieran revisión, influenciándose de la actividad de cada
paciente [5,12].
Es de tener en cuenta que en la osteonecrosis la remodelación
ósea esta alterada, lo que podría perjudicar la disponibilidad
de tejido óseo para fijar el implante, así como la posibilidad de
que se extienda la lesión, resultando en un apoyo inadecuado
del fémur, aumentando el riesgo de hundimiento y fracaso. En
este sentido, los pacientes jóvenes candidatos para artroplastia
tendrían un riesgo de fracaso aumentado dado su mayor nivel
de actividad, sumado a las restricciones de longevidad de la
prótesis, sin embargo, se deben balancear los beneficios sobre
los riesgos y la mejoría en la calidad de vida, que no contraindica
el procedimiento en pacientes jóvenes [5,12].
CONCLUSION
Finalmente se resaltan ciertos puntos claves que para el
médico son esenciales tener en cuenta, deducido en el análisis
exhaustivo de los estudios citados en esta actualización de NCF;
No se han identificado etiologías claras. El diagnóstico de la
enfermedad en etapas tempranas se hace con dificultad debido
a la escasa manifestación clínica en su inicio, por esto se debe
tener en cuenta dolor en ingle, glúteo o muslo de forma crónica
y descartar con pruebas complementarias sugeridas por las
clasificaciones diagnósticas.
Aun con clasificaciones distintas y variadas existe una ausencia
de concesos globales en referencia a una clasificación que resulte
ser práctica, sencilla y adecuada, sin embargo, se concluyó que
el método diagnóstico adecuado es la clasificación ARCO debido
a su incorporación de diversas imágenes, siendo esta una de las
más completas ya que une los modelos ficat y arlet con steinberg,
sin embargo, se recomienda como método de imagen diagnóstica la RMN, siendo su sensibilidad (88-100%), es una herramienta
muy útil para realizar el diagnóstico.
Con respecto a su tratamiento, es recomendable en caso de
estadios tempranos la descompresión de núcleo, por ser una
opción, con una tasa de éxito satisfactoria y una intervención
mínimamente invasiva. Ahora bien, en caso de estadio avanzado,
donde la articulación se encuentra colapsada y necrótica de
forma importante, la opción a considerar sería una artroplastia
total de cadera.
Conflicto de Intereses
Ninguno por declarar.
Referencias
- Alvarez López A, García Lorenzo Y. Clasificación y diagnóstico de la osteonecrosis de cabeza femoral. Rev Cuba de Ortop y Traumatol. 2005; 19(1).
Google Scholar
- Arbab D, König DP. Atraumatic femoral head necrosis in adults: Epidemiology, etiology, diagnosis and treatment. Dtsch Arztebl Int. 2016; 113(3): 31.
Indexed at, Google Scholar, Cross Ref
- Baig SA, Baig MN. Osteonecrosis of the femoral head: Etiology, investigations, and management. Cureus. 2018; 10(8).
Indexed at, Google Scholar, Cross Ref
- Barbhaiya M, Dong Y, Sparks JA, Losina E, Costenbader KH, Katz JN. Administrative Algorithms to identify Avascular necrosis of bone among patients undergoing upper or lower extremity magnetic resonance imaging: A validation study. BMC Musculoskelet Disord. 2017; 18(1): 1-6.
Indexed at, Google Scholar, Cross Ref
- Castigloini A, Singerman L, Brance ML. Osteonecrosis no traumática de cabeza femoral: Patogénesis, diagnóstico y tratamientos actuales. Actual En Osteol. 2015; 11(1): 57-70.
Google Scholar
- Chang C, Greenspan A, Beltran J, Gershwin ME. Osteonecrosis. Kelley and Firestein's Textbook of Rheumatol. 2017; 1764-1787.
Google Scholar
- Grecula MJ. CORR Insights®: Which Classification System Is Most Useful for Classifying Osteonecrosis of the Femoral Head?. Clin Orthop Relat Res. 2018; 476(6): 1250-1252.
Indexed at, Google Scholar, Cross Ref
- Hevia MM, Buil PR, Díaz MD, García AM, Quílez MV. La necrosis ósea avascular: Una enfermedad con nombre y apellidos: Una enfermedad con nombre y apellidos. Seram. 2018.
Google Scholar
- Hsu H, Nallamothu SV. Hip Osteonecrosis. Statperals publishing. 2020.
Indexed at, Google Scholar
- Jones LC, Mont MA, Collins KA. Clinical manifestations and diagnosis of osteonecrosis (avascular necrosis of bone). 2020.
Google Scholar
- Jones LC, Mont MA, Collins KA. Treatment of nontraumatic hip osteonecrosis (avascular necrosis of the femoral head) in adults. 2020.
Google Scholar
- Lespasio MJ, Sodhi N, Mont MA. Osteonecrosis of the hip: A primer. Perm J. 2019; 23: 18-100.
Indexed at, Google Scholar, Cross Ref
- Liu LH, Zhang QY, Sun W, Li ZR, Gao FQ. Corticosteroid-induced osteonecrosis of the femoral head: detection, diagnosis, and treatment in earlier stages. Chin Med J. 2017; 130(21): 2601-2607.
Indexed at, Google Scholar, Cross Ref
- Moya-Angeler J, Gianakos AL, Villa JC, Ni A, Lane JM. Current concepts on osteonecrosis of the femoral head. World J Orthop. 2015; 6(8): 590-601.
Indexed at, Google Scholar, Cross Ref
- Páramo CA, Sandí LA, Oliva JA. Necrosis avascular de cabeza femoral. Revista médica sinergia. 2020; 5(7): 1-2.
Google Scholar
- Bruguera PJ. Necrosis avascular de la cabeza femoral como secuela del tratamiento de la luxacion congenita de cadera. Reciamuc. 4(1): 4-14.
Google Scholar
- Shah KN, Racine J, Jones LC, Aaron RK. Pathophysiology and risk factors for osteonecrosis. Curr Rev Musculoskelet Med. 2015; 8(3): 201-209.
Indexed at, Google Scholar, Cross Ref
- Sultan AA, Mohamed N, Samuel LT, Chughtai M, Sodhi N, Krebs VE, Stearns KL, Molloy RM, Mont MA. Classification systems of hip osteonecrosis: An updated review. Int Orthop. 2019 May; 43(5): 1089-1095.
Indexed at, Google Scholar, Cross Ref
- Takashima K, Sakai T, Hamada H, Takao M, Sugano N. Which classification system is most useful for classifying osteonecrosis of the femoral head?. Clin Orthop Relat Res. 2018; 476(6): 1240-1249.
Indexed at, Google Scholar, Cross Ref
- Tripathy SK, Goyal T, Sen RK. Management of femoral head osteonecrosis: Current concepts. Indian J Orthop. 2015; 49(1): 28-45.
Indexed at, Google Scholar, Cross Ref
- Yoon BH, Mont MA, Koo KH, Chen CH, Cheng EY, Cui Q, et al. The 2019 revised version of association research circulation osseous staging system of osteonecrosis of the femoral head. J Arthroplasty. 2020; 35(4): 933-940.
Indexed at, Google Scholar, Cross Ref
- Zhao DW, Yu M, Hu K, Wang W, Yang L, Wang BJ, et al. Prevalence of nontraumatic osteonecrosis of the femoral head and its associated risk factors in the Chinese population: Results from a nationally representative survey. Chin Med J. 2015; 128(21): 2843-2850.
Indexed at, Google Scholar, Cross Ref






